• Danfeng Lin, • Lesang Shen, • Meng Luo, • Kun Zhang, • Jinfan Li, • Qi Yang, • Fangfang Zhu, • Dan Zhou, • Shu Zheng, • Yiding Chen & • Jiaojiao Zhou
Transdukcia signálu a cielená terapia objem 6 , Číslo článku: 404 ( 2021 ) Citovať tento článok
• 70 000 prístupov
• 358 citácií
• 87 Altmetric
• Metrikypodrobnosti
Abstraktné
Cirkulujúce nádorové bunky (CTC) sú nádorové bunky, ktoré sa oddelili od primárneho nádoru a extravazujú do krvi a cirkulujú v krvi. Pochopenie metastatickej kaskády CTC má obrovský potenciál na identifikáciu cieľov proti rakovinovým metastázam. Detekcia týchto veľmi zriedkavých CTC medzi masívnymi krvnými bunkami je náročná. Nové technológie na detekciu CTC však výrazne prispeli k prehĺbeniu výskumu biológie CTC a uľahčili ich klinickú aplikáciu. Súčasné technológie na detekciu CTC sú tu zhrnuté spolu s ich výhodami a nevýhodami. Detekcia CTC je zvyčajne závislá od molekulárnych markerov, pričom adhézna molekula epiteliálnych buniek je najpoužívanejšia, hoci molekulárne markery sa medzi rôznymi typmi rakoviny líšia. V CTC boli identifikované vlastnosti spojené s epitelovým-mezenchymálnym prechodom a kmeňovosťou, čo naznačuje ich zvýšenú metastatickú kapacitu. Len malá časť CTC môže prežiť a prípadne iniciovať metastázy, čo naznačuje, že interakcia a modulácia medzi CTC a nepriateľským krvným mikroprostredím je nevyhnutná pre metastázy CTC. Jednobunkové sekvenovanie CTC bolo rozsiahle skúmané a umožnilo výskumníkom odhaliť genóm a transkriptóm CTC. V tomto dokumente tiež skúmame klinické aplikácie CTC, najmä na monitorovanie odpovede na liečbu rakoviny a pri hodnotení prognózy. Preto CTC majú a budú naďalej prispievať k poskytovaniu významných poznatkov o metastatických procesoch a otvoria nové cesty pre užitočné klinické aplikácie.
Podobný obsah si prezerajú ostatní
Článok 9. decembra 2022
Článok 2. júna 2023
Článok Otvorený prístup2. októbra 2019
Úvod
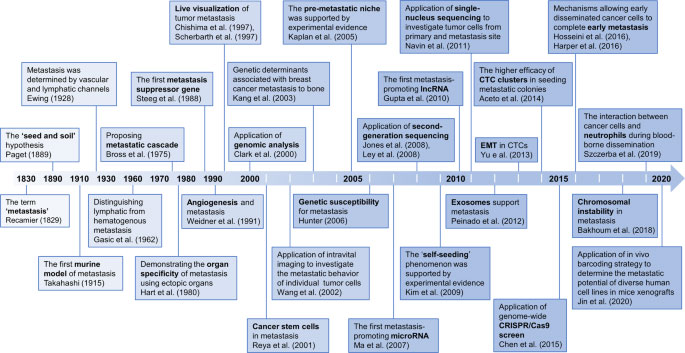
Metastázy sú najsmrteľnejším znakom rakoviny 1 . Napriek významnému vývoju v diagnostike a liečbe rakoviny v posledných storočiach zostávajú metastázy hlavnou prekážkou zlepšenia klinických výsledkov u pacientov s rakovinou 2 . Napriek tomu sme za posledných dvesto rokov boli svedkami významného pokroku v odhaľovaní základných konceptov, ktoré sú základom vývoja metastáz, a vo vytváraní nových technológií na uľahčenie výskumu metastáz rakoviny. Obr . 1 zdôrazňuje kľúčové objavy a míľniky v štúdiu metastáz rakoviny. Hypotéza „semena a pôdy“ Stevena Pageta 3 z 30. rokov 19. storočia názorne objasnila postup metastázovania rakoviny. S pokrokom vedy a technológií, najmä od roku 2000, sa vyvinulo množstvo nových technológií, ako napríklad vysokovýkonné sekvenovanie 4 , 5 , modely transgénnych myší 6 , editačné nástroje CRISPER/Cas9 7 a jednobunkové sekvenovanie 8 . Vďaka týmto výkonným technológiám sa biologické javy, ktoré sú základom metastáz, ako je epitelovo-mezenchymálny prechod (EMT) nádorových buniek 9 , úloha exozómov pri podpore metastáz 10 , cirkulujúce nádorové bunky (CTC) a zhluky CTC pri očkovaní metastatických kolónií 11 a komplexné interakcie medzi nádorovými bunkami a mikroprostredím 12 sa postupne odmaskovali spolu s objavom mnohých hnacích génov súvisiacich s metastázami. „Čierna skrinka“ metastáz sa postupne odhaľuje a predpokladá sa, že v blízkej budúcnosti budú na obzore účinné látky zacielené na metastázy.
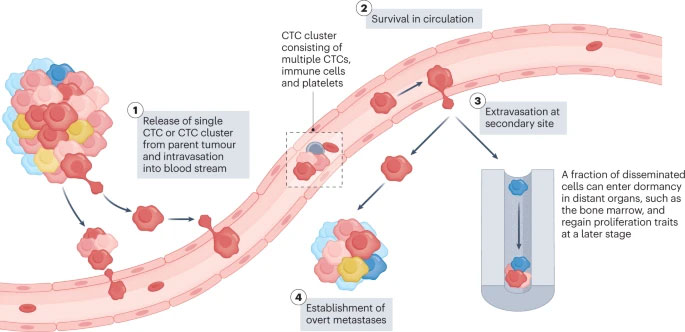
Rakovinové metastázy sú komplexný viacstupňový proces zahŕňajúci inváziu rakovinových buniek do primárneho miesta, intravazáciu do obehu, prežitie v obehu, extravazáciu z obehu a pripojenie a kolonizáciu metastatického miesta (obr. 2 ). CTC sú definované ako nádorové bunky, ktoré sa oddelili z primárneho nádoru a sú odplavené obehovým alebo lymfatickým systémom. Doteraz sa väčšina výskumov CTC zameriavala na CTC v krvnom obehu. CTC boli prvýkrát opísané v roku 1869 Ashworthom, ktorý pozoroval „niektoré bunky“ v krvi pacienta s metastatickým karcinómom, ktorý mal podobný vzhľad ako nádorové bunky v primárnych nádoroch 13 . Predpokladá sa, že CTC sú substrátom metastáz. Hoci CTC pochádzajú z primárneho nádoru, odlišujú sa od primárnych nádorových buniek 14 , s prechodovými vlastnosťami EMT, ktoré im pomáhajú oslobodiť sa od primárneho nádoru a uľahčujú intravazáciu do krvného obehu, šírenie v zhlukoch CTC na zvýšenie metastatického potenciálu a prejavujú stopku. vlastnosti, ktoré zvyšujú ich schopnosť iniciovať metastázy (obr. 2 ). Väčšina CTC však zahynie v obehu a iba obmedzené CTC prežijú a infiltrujú vzdialené orgány. Interakcie medzi CTC a krvným prostredím (obr. 2 ), vrátane toho, ako CTC unikajú imunitnému dohľadu v krvi, sa široko podieľajú na metastatických mechanizmoch CTC. Trvalo viac ako storočie, kým výskumníci rozpoznali kritickú úlohu CTC pri metastázovaní rakoviny kvôli jedinečným technickým výzvam potrebným na izoláciu týchto veľmi vzácnych CTC z masívnej zásoby cirkulujúcich krviniek 15 . V posledných dvoch desaťročiach však nové technológie na izoláciu CTC umožnili výskum biológie CTC a uľahčili klinické aplikácie CTC pri skríningu rakoviny, monitorovaní odpovede na liečbu a hodnotení prognózy.
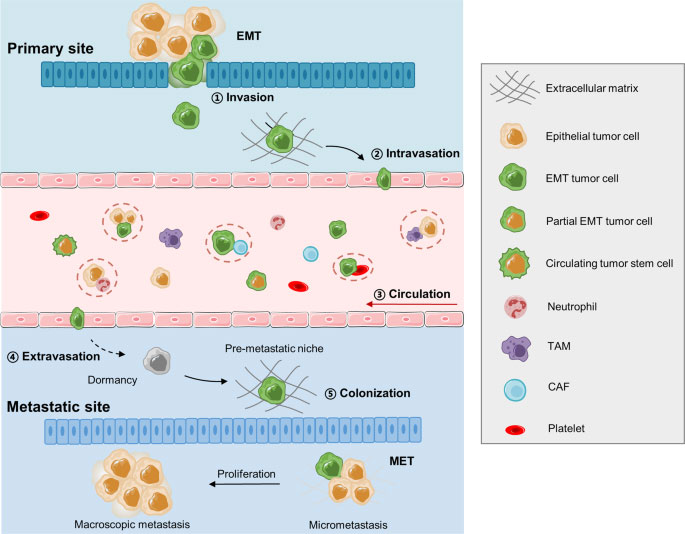
Viacstupňový proces metastázovania rakoviny. Komplexný metastatický proces zahŕňa inváziu nádorových buniek do primárneho miesta, intravazáciu do obehu, prežitie v obehu ako CTC a interakciu s krvnými bunkami, extravazáciu z obehu, pripojenie a kolonizáciu metastatického miesta. EMT: prechod z epitelu na mezenchymálny, CAF: fibroblast spojený s rakovinou, TAM: makrofág spojený s nádorom.
V tomto prehľade je plne preskúmaná biológia CTC, ako aj ich interakcia s mikroprostredím krvi. Okrem toho bude zhrnutý rastúci počet vysoko sofistikovaných technológií na obohacovanie a izoláciu CTC. Nakoniec diskutujeme aj o obrovskom potenciáli CTC v klinických aplikáciách.
Biológia CTC
Molekulárna charakterizácia CTC
Experimentálne dôkazy podporili názor, že nádorové bunky sa môžu šíriť aj počas skorých štádií vývoja nádoru16,17 . Molekulárna charakterizácia CTC pridá poznatky k základnému mechanizmu metastatických procesov, čím prispeje k včasnej diagnóze a prevencii metastáz.
Molekulové markery CTC
Panel molekulárnych markerov sa použil na detekciu CTC pri rôznych rakovinách. CTC-asociované markery používané pre rôzne rakoviny sú zhrnuté v tabuľke 118,19 . Keďže väčšina rakovín je epitelového pôvodu, najbežnejším markerom používaným pre CTC je EpCAM, „univerzálny“ epiteliálny marker rakovín20 . Expresia EpCAM sa líši medzi rôznymi typmi rakoviny 21 a technológie detekcie CTC založené na EpCAM sa široko používajú pri rakovinách, ktoré silne exprimujú EpCAM, ako je rakovina prsníka a prostaty. Mnohé štúdie ukázali, že CTC pri rakovine prsníka a prostaty sú EpCAM-pozitívne a potvrdili ich prognostickú hodnotu v prípadoch skorého alebo metastatického štádia22,23 . Iné typy rakoviny odvodené od epitelu, ako napríklad rakovina pankreasu24 , kolorektálna rakovina25 a hepatocelulárna rakovina26 , majú tiež značnú mieru detekcie EpCAM-pozitívnych CTC. Podobne prítomnosť týchto EpCAM-pozitívnych CTC predpovedá skoré vzdialené metastázy a horšie prežívanie pacientov 25 , 27 , 28 . Použitie EpCAM ako CTC markera má však obmedzenia. Nemôže sa použiť v nádoroch, ktoré sú EpCAM-negatívne alebo s nízkou expresiou, ako sú neurogénne rakoviny. CTC môžu podstúpiť EMT a epitelové markery, vrátane EpCAM, sú počas EMT regulované smerom nadol, čo ovplyvňuje mieru detekcie EpCAM-pozitívnych CTC. Hoci existujú pochybnosti o tom, či sú technológie založené na EpCAM vhodné na detekciu všetkých CTC, početné štúdie ilustrovali potenciálnu hodnotu EpCAM-pozitívnych CTC v klinických aplikáciách 29 . Do určitej miery sú EpCAM-pozitívne CTC podstatnou podskupinou všetkých CTC, takže EpCAM-pozitívne CTC by stále mohli byť spoľahlivým biomarkerom, ak je prognóza rakoviny a terapeutická účinnosť relevantná pre EpCAM-pozitívne CTC.
Tabuľka 1 Molekulárne markery používané na identifikáciu CTC
V dôsledku EMT aktivity niektorých epiteliálnych rakovinových buniek detegovanie iba EpCAM-pozitívnych CTC pravdepodobne podhodnocuje skutočnú celkovú populáciu CTC a chýba dôležité biologické informácie o EpCAM-negatívnych CTC. Pri niektorých typoch rakoviny, ako sú pacienti s nemalobunkovým karcinómom pľúc (NSCLC), sa dokonca zistilo, že množstvo EpCAM-negatívnych CTC bolo významne väčšie ako EpCAM-pozitívnych CTC30 . Zlá izolácia CTC technológiami založenými na EpCAM sa však dá zachrániť použitím epiteliálnych aj mezenchymálnych markerov rakoviny, ako aj detekčných metód nezávislých od markerov. Napríklad pri rakovine prsníka použitie fluorescenčných magnetických nanočastíc pozostávajúcich z rozhrania s dvojitou protilátkou zacieleného na EpCAM aj N-kadherín prispelo k vysoko účinnej izolácii a rýchlej identifikácii CTC31,32 . Pri rakovine žlčových ciest umožnil jednobunkový test na detekciu CTC identifikáciu epitelových CTC aj nekonvenčných CTC, ktorým chýbali epiteliálne a leukocytové markery, a preto viedol k zvýšeniu miery pozitivity CTC33 . Program EMT rakovinových buniek vykazuje molekulárne zmeny, vrátane zníženej expresie epitelových markerov (E-kadherín, ZO-1, klaudíny a okludíny) a zvýšenej expresie mezenchymálnych markerov (vimentín, N-kadherín, fibroblast-špecifický proteín1 a fibronektín ) 34 . EMT sa vykonáva transkripčnými faktormi súvisiacimi s EMT, ktoré patria najmä do rodín SNAIL, TWIST a ZEB34 . Všetky tieto molekuly súvisiace s EMT možno teoreticky použiť na metódy zacielenia EMT-CTC. Mnohé molekuly súvisiace s EMT sú však cytoplazmatické alebo jadrové proteíny, čo vylučuje ich použitie v v súčasnosti dostupných technológiách detekcie CTC založených na membránových molekulách. Proteíny ako E-kadherín, vimentín a twist boli najčastejšie používané v minulosti 35 (tabuľka 1 ), pravdepodobne kvôli ich dostupnosti detekcie v tradičných CTC detekčných technológiách vrátane triedenia prietokovou cytometriou, imunofarbenia a fluorescenčnej in situ hybridizácie (FISH ) farbenie. Vznik jednobunkových CTC sekvenčných technológií 36 však umožní komplexnejšie demaskovať stav EMT CTC a môže pokryť všetky molekulárne zmeny súvisiace s EMT na úrovni RNA.
Iné biomarkery, ako je ľudský receptor epidermálneho rastového faktora-2 (HER2) 37 , 38 , 39 , 40 , 41 , 42 , 43 , 44 , 45 , 46 , 47 , estrogénový receptor 39 , 48 , 49 , 50 špecifický pre prostatu membránový antigén 51 , 52 , 53 , folátový receptor 54 , 55 , 56 a survivín 57 , boli opísané ako CTC markery pri rôznych rakovinách s rôznym klinickým významom. Tieto CTC markery špecifické pre rakovinu sú uvedené v tabuľke 1 . Väčšina týchto CTC markerov špecifických pre rakovinu je v súlade so špecifickými molekulárnymi markermi primárneho nádoru. Existuje však nesúlad v expresii špecifických markerov medzi primárnym nádorom a CTC. Napríklad miera nesúladu amplifikácie génu HER2 medzi CTC a primárnym nádorom prsníka bola okolo 15 % 58 , čo naznačuje klonálnu selekciu CTC alebo klonálnu akvizíciu, pravdepodobne v dôsledku genetickej nestability. Malo by sa spomenúť, že v prípade melanómu, rakoviny kože, ktorá začína v melanocytoch, sú technológie detekcie CTC založené na niekoľkých adhéznych molekulách melanómových buniek, ako sú HMW-MAA 59 , 60 , 61 , MART-1 62 , 63 , 64 , CD14661,65 a MAGE A362,63,66 , čo sú veľmi špecifické molekulárne markery pre melanóm .
Rozmanitosť markerov CTC naznačuje heterogenitu CTC medzi rôznymi typmi rakoviny. Dokonca aj u jedného pacienta sú CTC priestorovo-časovo heterogénne, čo môže byť výsledkom priestorovo odlišného mikroprostredia v krvi a časových zmien v terapeutickej odpovedi. Preto je ťažké definovať celú populáciu CTC pomocou veľmi obmedzených molekulárnych markerov, ktoré sú v súčasnosti dostupné. Okrem toho by CTC markery nemali byť konštantné medzi rôznymi štádiami rakoviny a obdobiami liečby.
Analýza genómu CTC
Genomická nestabilita prispieva k evolúcii nádoru a vzniku rezistentných nádorových subklonov. Monitorovanie genómovej nestability nádoru, najmä z hľadiska nádorovej rezistencie a metastáz, výrazne prispieva k hodnoteniu odpovede na liečbu a precíznej medicíne. Vyhodnotenie hodnotenia CTC pomocou neinvazívnej tekutej biopsie je dostupné pre sériové odbery vzoriek na detekciu genómovej nestability nádoru.
Určenie stavu mutácií EGFR a KRAS je kľúčové pre vedenie liečby u pacientov s NSCLC, ktorí dostávajú inhibítory tyrozínkinázy EGFR, a u pacientov s kolorektálnym karcinómom liečených anti-EGFR terapiou. Veľkú pozornosť pritiahla zhoda mutácií medzi CTC a zodpovedajúcim primárnym alebo metastatickým nádorovým tkanivom. Pomocou mikrofluidnej techniky na zachytenie CTC, Maheswaran et al. zistili , že iba dvaja z 31 pacientov s mutáciami boli z ich detekčného testu prehliadnutí67 . Identifikovali aktivačnú mutáciu EGFR v CTC u 92 % metastatických pacientov s NSCLC a zistili mutáciu T790M rezistentnú na liek v CTC u 33 % pacientov, ktorí reagovali na liečbu inhibítorom tyrozínkinázy, a u 64 % pacientov, ktorí vykazovali klinickú progresiu67 . Na analýzu mutácie génu KRAS sa miera zhody mutácií medzi CTC a zodpovedajúcimi primárnymi nádormi pohybovala od 37 % do 90 % v prípadoch kolorektálneho karcinómu 68 , 69 , 70 , 71 . Tento rozdiel v miere zhody môže byť spôsobený rôznymi protokolmi výberu CTC použitými v týchto štúdiách. Mutácie KRAS sú bežné aj pri pankreatickom duktálnom adenokarcinóme (PDAC), prítomných v 90 % prípadov PDAC. Kulemann a spol. zistili, že miera nesúladu mutácie KRAS v CTC a zodpovedajúcich nádoroch PDAC bola 42 % 72 . Štúdie analýzy génových mutácií v CTC sa uskutočnili aj pri mnohých rakovinách, ako je rakovina prostaty 73 , 74 , rakovina prsníka 75 , 76 , hepatocelulárne karcinómy 77 a často sa zistila mutačná nezhoda medzi CTC a zodpovedajúcimi nádormi. Miera nesúladu bola pravdepodobne pripísaná odlišnej účinnosti detekcie mutácií CTC alebo heterogenite medzi CTC a primárnymi nádorovými bunkami. Genomické hodnotenie nádorového tkaniva a CTC môže byť komplementárne. Takže kombinácia mutačného testovania CTC a vzoriek nádorov by presnejšie usmerňovala liečbu.
Určenie zmien počtu kópií (CNA) CTC pomáha analyzovať a sledovať profily rakoviny, keď sa nádory vyvíjajú. Pri rakovine pľúc Ni a spol. 78 zistili, že CTC vykazujú reprodukovateľné vzory CNA, podobné vzorom metastatických nádorov, a rôzni pacienti zdieľali podobné vzory CNA. V prípade malobunkového karcinómu pľúc klasifikátor pre CTC založený na CNA správne priradil 83,3 % pacientov ako chemorefraktérnych alebo chemosenzitívnych 79 . Pri rakovine prsníka je hodnotenie CNA v archivovaných CTC uskutočniteľné. Paoletti a kol. 80 zistili, že CNA CTC a spárované metastatické nádorové tkanivo u pacientov s rakovinou prsníka boli vysoko zhodné, hoci CTC a zodpovedajúce nádorové tkanivo obsahovali niekoľko nezhodných zmien v počte kópií, čo naznačuje, že CTC boli subklonové bunky nádorových tkanív. Pri trojnásobne negatívnej rakovine prsníka sú CTC s chromozómom 10 a 21q CNA prediktívne pre klinickú progresiu a ich sieťová analýza predstavila prepojené moduly vrátane signalizácie HER/fosfatidylinozitol-4,5-bisfosfát 3-kinázy/RAS/ JAK81 . Pri rakovine prostaty Lambro a spol. 82 odhalili, že CNA CTC boli medzi pacientmi a medzibunkovými heterogénnymi a mohli byť vynechané v analýzach hromadnej biopsie. Pri metastatickej kastrácii rezistentnej rakovine prostaty analýza počtu kópií celého genómu CTC ukázala, že bežné genómové zisky v CTC zahŕňali gény, ako je androgénny receptor (AR), mezenchymálny-epiteliálny prechod (MET), ERG a cyklín-dependentná kináza 12 , zatiaľ čo bežné genómové straty boli pozorované v génoch, ako je homológ fosfatázy a tenzínu (PTEN), RAF1 a GATA283 . Podobne Malihi a kol. tiež pozorovali, že CNA v génoch vrátane PTEN, RB1, TP53 a AR úzko súvisia s genómovou nestabilitou a prežitím pri agresívnom variante rakoviny prostaty84 .
V CTC sa uskutočnili aj iné analýzy genómu. Testovanie FISH bolo prijaté v CTC na detekciu biomarkerov citlivosti na liečbu, ako je testovanie ALK FISH v CTC pacientov s NSCLC85 a testovanie HER2 FISH v CTC pacientov s rakovinou prsníka86,87 . Nedávno sa na základe techniky analýzy metylácie DNA s jednobunkovým rozlíšením odhalil metylóm DNA jednotlivých CTC a CTC klastrov u pacientov s rakovinou prsníka a naznačil, že získaný hypometylačný profil CTC klastrov bol spojený so zlou prognózou a že liečba Inhibítory Na+/K+-ATPázy na disociáciu CTC klastrov by mohli zvrátiť metylačný profil CTC klastrov a potlačiť metastázy88 .
Transkriptómová analýza CTC
Jednobunkové sekvenovanie sa v posledných rokoch rýchlo rozvinulo a použilo sa na skúmanie transkriptómov CTC. Jednobunkové expresné profily môžu odlíšiť CTC od mezoteliálnych buniek a krvných buniek v pľúcnom adenokarcinóme, s reprezentatívnymi markermi vrátane EpCAM pre CTC89 . Analýza transkriptómu založená na jednobunkovom sekvenovaní odhalila heterogenitu v subpopulácii CTC. Testovaním expresie génov spojených s proliferáciou, ako je proliferačný marker Ki-67, Magbanua et al90 . zistili, že 65 % CTC u pacientov s metastatickým karcinómom prsníka malo nízku proliferáciu Ki-67 a že 35 % pacientov s vysokou proliferáciou expresie Ki-67 malo zlú prognózu. Cheng a kol. 91 vykonali jednobunkovú transkriptómovú analýzu 666 CTC u pacientov s metastatickým karcinómom prsníka. Zistili, že intra-pacientské CTC boli heterogénne, pokiaľ ide o stavy podobné EMT a MET, a CTC boli obohatené o fenotyp podobný kmeňu91 . Jednobunkové sekvenovanie CTC tiež výrazne pomohlo pri objavovaní signálnych dráh vodičov, ktoré prispeli k metastázam a zlyhaniu liečby. RNA-Seq jedného CTC prostaty indikovala aktiváciu nekanonickej Wnt signalizácie u pacientov rezistentných na antiandrogén92 . Ďalej, s použitím myšacích modelov, ektopická expresia Wnt5a zoslabila účinky AR inhibítora a supresia Wnt5a by mohla čiastočne obnoviť citlivosť buniek rakoviny prostaty rezistentných na liečivo92 . CTC boli spojené so zlou prognózou pri kolorektálnom karcinóme. Štúdia CTC-špecifického transkriptómového profilu 93 u šiestich pacientov s metastatickým kolorektálnym karcinómom charakterizovala 410 CTC-špecifických génov, ktoré primárne súviseli s bunkovým pohybom a adhéziou, ako je VCL ITGB5, kostný morfogenetický proteín 6, transformujúci rastový faktor beta 1 a talín 1 a súviseli s bunkovou smrťou a proliferáciou, ako je prekurzorový proteín amyloidu beta, klusterín a TIMP1.
Epitelový-mezenchymálny prechod CTC
EMT je proces, pri ktorom epitelové nádorové bunky strácajú svoju medzibunkovú adhéziu a získavajú mezenchymálne a invazívne vlastnosti. Počas šírenia sa nádorové bunky oddeľujú od bazálnej membrány prostredníctvom aktivácie EMT a priamo vstupujú do obehu, pričom slúžia ako CTC putujúce do vzdialených miest. Keď CTC extravazujú, podstúpia reverzný proces nazývaný MET a proliferujú za vzniku makrometastáz94,95,96 . Metastatický vývoj tu závisí od jemnej rovnováhy prechodu medzi týmito dvoma fenotypmi. Činnosť EMT-MET bola tiež navrhnutá tak, aby zohrávala dôležitú úlohu v metastatickom procese CTC97 . Pomocou myších modelov sa zistilo, že CTC epitelového typu s obmedzeným mezenchymálnym prechodom mali najsilnejšiu kapacitu tvorby pľúcnych metastáz, zatiaľ čo CTC mezenchymálneho typu vykazovali obmedzenú metastatickú schopnosť98 . Pri rakovine prsníka CTC vykazujú dynamické zmeny v zložení EMT a zistilo sa, že mezenchymálne CTC sú úzko spojené s progresiou rakoviny9,98 . Množstvo štúdií ukázalo zvýšenú EMT CTC skôr ako primárnych nádorových buniek pri rôznych rakovinách99 , 100 , 101 , 102 , 103 . V štúdii založenej na bioinformatickej analýze siedmich súborov génových čipov Guan a kol. ukázali, že v porovnaní s primárnymi nádormi sa hlavné zmeny v CTC týkali bunkovej adhézie, EMT a apoptózy104 . V prospektívnej štúdii zahŕňajúcej 39 pacientok s invazívnym karcinómom prsníka Tashireva et al. pozorovali väčšinu heterogénnych CTC fenotypov (22 z 24 detegovateľných vzoriek) vykazujúcich plasticitu EMT105 . Zaujímavé je, že sa zistilo, že šmykové napätie tekutiny môže indukovať EMT CTC prostredníctvom JNK signalizácie pri rakovine prsníka, čo ďalej potvrdilo vzťah medzi rozšíreným EMT CTC a zlým prežitím pacientov 106 .
Klinicky môže byť kombinácia celkového počtu CTC a podielu mezenchymálnych CTC107 použitá na monitorovanie terapeutickej rezistencie a predpovedanie prognózy u pacientov s rakovinou v dôsledku významných rozdielov v prežívaní tohto kritéria108 . Napríklad, keďže základná prítomnosť celkových CTC pri pokročilom NSCLC poskytla zlú prognózu109 a prítomnosť viac ako piatich EMT-CTC indikovala progresívne ochorenie110 . Zistilo sa, že rôzne počty celkových CTC a EMT CTC hrajú dôležitú úlohu pri určovaní prognózy pacientov s rakovinou prsníka. Je zaujímavé, že sa zdôraznilo, že lepšie pochopenie podtypov EMT-CTC a ich interakcií s mononukleárnymi bunkami periférnej krvi by mohlo pomôcť navrhnúť lepšie antimetastatické liečby111 . Keďže CTC EMT-pozitívni pacienti s pomerom neutrofilov k lymfocytom ≥3 mali 8,6-krát zvýšené riziko recidívy ochorenia v porovnaní s CTC EMT-negatívnymi pacientmi s nižšími hladinami neutrofilov, skóre založené na zápale zvýšilo prognostickú hodnotu CTC pri primárnom karcinóme prsníka 112 . Preto zacielenie na dráhu EMT môže zabrániť šíreniu nádorových buniek u pacientov v ranom štádiu a eradikovať metastatické bunky v pokročilých štádiách.
Stonka CTC
Mnoho predchádzajúcich štúdií naznačilo subpopuláciu agresívnych CTC so znakmi „stonky“ pri rôznych rakovinách, čo sa týka ich vlastností pre samoobnovu a indukciu rastu nádoru. Pri rakovine močového mechúra štúdie uvádzajú vysokú expresiu OCT4, kľúčového proteínu udržiavajúceho kmeň113 , v podskupine CTC114 . Pri rakovine prsníka sa uvádza, že fenotypy buniek CD44 + /CD24- /low a aldehyddehydrogenázy 1 (ALDH1)+ sú spojené s kmeňovosťou. Po detekcii expresie CD44, CD24 a ALDH1 CTC u 30 pacientov s metastatickým karcinómom prsníka Theodoropoulos et al. zistili, že 35,2 % z 1439 CTC bolo CD44 + /CD24- /nízke a 17,7 % z 238 CTC bolo ALDH1 vysoké /CD24- /nízke , čo poskytuje dôkaz o kmeňovosti CTC96 . Bunková línia CTC-3 vytvorená z buniek periférnej krvi pacienta s rakovinou prsníka vykazovala agresívnejší rast ako široko používaná bunková línia rakoviny prsníka MCF-7. Génové profilovanie odhalilo vyššiu expresiu kmeňových markerov v bunkovej línii CTC-3 v porovnaní s bunkami MCF- 7115 . Pri hepatocelulárnom karcinóme (HCC) bolo 71,4 % pacientov s HCC CTC pozitívnych na marker rakovinových kmeňových buniek, CD44; mali teda významnú populáciu CTC s kmeňovými vlastnosťami, ktoré by mohli prispieť k prežitiu a šíreniu nádorových buniek116 . V glioblastóme analýza RNA-seq odhalila kmeň a chemorezistenciu v CTC117 indukovanú aktiváciou Wnt . Pri rakovine prostaty bol marker kmeňových buniek CD133 pozorovaný u väčšiny (> 80 %) CTC pacientov s metastatickým karcinómom prostaty rezistentným na kastráciu 97 a kmeňová subpopulácia CXC motívu chemokínového receptora 4+/CD133+CTCs bola viac prevláda v EpCAM-negatívnych CTC ako v EpCAM-pozitívnych CTC118 .
Je dôležité porozumieť mechanizmom regulujúcim kmeň CTC a interferencia s vlastnosťami kmeňa subpopulácie CTC môže účinnejšie potlačiť progresiu a relaps rakoviny. CTC podliehajú značným úrovniam šmykového toku tekutiny počas ich šírenia a samotný šmykový tok tekutiny môže mať vplyv na CTC. Použitím modelu rakoviny prsníka s metastázami v mozgu sa navrhlo, že hemodynamický šmykový tok by mohol upregulovať kmeňové gény CTC pri prežívaní v podmienkach šmykového toku119 . Prechod CTC podobný EMT prostredníctvom downregulácie signalizácie ERK a GSK3p by mohol podporiť konverziu CTC na kmeňové CTC s vysokou schopnosťou vytvárať sféry a iniciovať nádor120.
CTC a krvné mikroprostredie
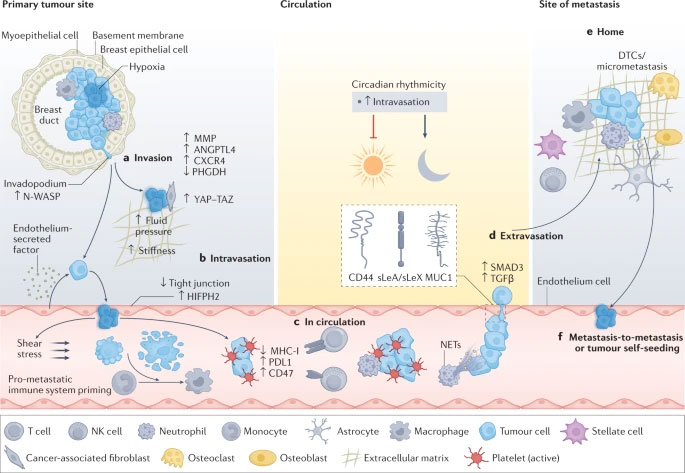
Keď sú transportované v krvnom riečisku, väčšina CTC je obmedzená škodlivým šmykovým stresom alebo zomrie na anoikis, mechanizmus programovanej bunkovej smrti v dôsledku straty bunkovej väzby121,122 . Len malá časť CTC úzko interaguje s krvnými doštičkami, neutrofilmi , makrofágmi , myeloidnými supresorovými bunkami (MDSC) alebo fibroblastmi spojenými s rakovinou (CAF), aby unikli imunitnému systému a podporili ich prežitie123,124 . Nedávno hromadiace sa štúdie naznačujú, že interakcia a modulácia medzi CTC a nepriateľským krvným mikroprostredím je nevyhnutná pre adhéziu k endotelovým bunkám, inváziu tkaniva a metastázy nádoru (obr. 3 ).
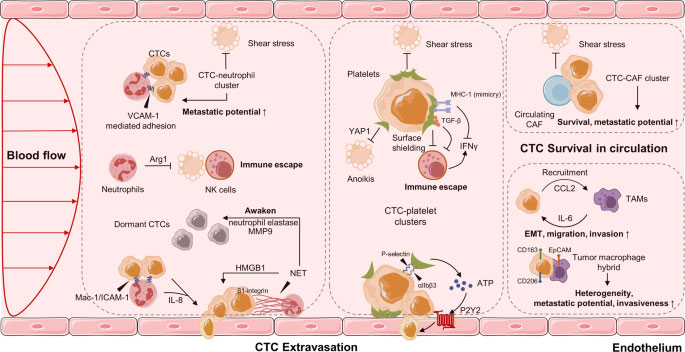
Interakcia CTC s neutrofilmi
Neutrofily sú najpočetnejšie cirkulujúce leukocyty u ľudí a nedávno boli študované na podporu progresie rakoviny125 . Zvýšený počet neutrofilov v obehu je spojený so zlou prognózou pri niekoľkých typoch rakoviny 126 , 127 , 128 . Tvorba zhlukov CTC-bielych krviniek (WBC) bola predtým hlásená v krvnom obehu 129 . V roku 2019 Szczerba a spol. určili, že CTC boli významne spojené s neutrofilmi u myších modelov aj u pacientov s rakovinou prsníka, pričom vykazovali väčší metastatický potenciál s väčšou expresiou génov, ktoré zahŕňajú progresiu bunkového cyklu v porovnaní so samotnými CTC130 . Tieto pozorovania sú v súlade s predchádzajúcimi zisteniami, ktoré ukazujú proliferačnú úlohu neutrofilov na nádorových bunkách131 . Väzba CTC a neutrofilov je sprostredkovaná bunkovým spojením a pravdepodobne vyžaduje adhéznu molekulu vaskulárnych buniek 1 130 . Okrem toho môžu neutrofily priamo adherovať na CTC prostredníctvom interakcie Mac-1/ICAM-1 a pôsobiť ako most medzi nádorovými bunkami a pečeňovým parenchýmom, čím podporujú extravazáciu a pečeňové metastázy132 . CTC sa teda zhlukujú s neutrofilmi ukotvenými vo vaskulárnom endoteli pre extravazáciu, pričom odolávajú šmykovému namáhaniu a proces je sprostredkovaný sériou bunkových adhéznych proteínov, ako je kadherín, integrín a povrchový glykoproteín133,134,135 . Je zaujímavé, že Chen a kol. zistili, že IL-8 vylučovaný z neutrofilov bol nevyhnutný pre sekvestráciu neutrofilov so zastavenými nádorovými bunkami a pre extravazačné správanie susedných nádorových buniek cez endoteliálnu bariéru136 .
Neutrofily môžu tiež podporovať metastázy nepriamo. Neutrofilné extracelulárne pasce (NET) sú sieťovité štruktúry tvorené komplexmi DNA-histón a proteínmi uvoľnenými z aktivovaných neutrofilov so schopnosťou ovplyvniť biológiu CTC 137 . Mnohé štúdie zistili , že NET boli schopné zachytiť CTC v obehu, a tým podporili metastatickú disemináciu138,139 . Experimenty in vitro a in vivo ukázali, že adhézia CTC k NET je sprostredkovaná p1-integrínom exprimovaným na NET aj rakovinových bunkách, pričom tento účinok bol zrušený po podaní DNAázy I139 . V myšom modeli chirurgického stresu spustila tvorba NET uvoľnenie vysokomobilného skupinového boxu 1, ktorý aktivoval TLR9-sprostredkované dráhy v CTC, a preto urýchlil progresiu pečeňových metastáz 140 . Okrem toho môžu NET tiež prebudiť spiace rakovinové bunky a podporovať metastázy. Nedávno Albrengues a spol. elegantne demonštrovali, že dve proteázy spojené s NET, neutrofilná elastáza a matricová metaloproteináza 9 (MMP9), sa koncentrujú na laminíne, provokujú jeho štiepenie vytvorením epitopu, ktorý indukuje prebudenie spiacich rakovinových buniek aktiváciou integrínu a signalizáciou FAK/ERK/MLCK/YAP 141 . Na druhej strane sa ukázalo, že proteín exprimovaný v nádore, ako je proteáza katepsín, podporuje pľúcne metastázy rakoviny prsníka tým, že podporuje tvorbu NET v metastatických výklenkoch142 . Coiled-coil doména obsahujúca proteín 25, ďalší proteín exprimovaný na membráne rakovinových buniek, by mohol slúžiť ako špecifický senzor pre komponent DNA NETs, ktorý indukuje migráciu a adhéziu nádorových buniek143 . Okrem toho, tvorbou NET môžu cirkulujúce neutrofily pomôcť CTC uniknúť imunitnému dohľadu potlačením aktivácie periférnych leukocytov144 , funkcie prirodzených zabíjačov (NK) buniek145 , protinádorovej odpovede efektorových T buniek146 a dokonca aj spoluprácou s inými imunitnými bunky (ako sú y5T bunky produkujúce IL17) 147 . Celkovo existujú dôkazy o prometastatickej úlohe neutrofilov v ich interakcii s CTC, ale konkrétny mechanizmus je potrebné podrobnejšie objasniť.
Interakcia CTC s makrofágmi
Makrofágy spojené s nádorom (TAM) nielen prispievajú k progresii metastáz v rámci primárneho nádoru, ale podporujú aj neskoršie štádiá metastáz vrátane šírenia a extravazácie CTC148 . Hamilton a kol. pokúsili skúmať interakcie CTC-makrofág spoločnou kultiváciou mononukleárnych buniek periférnej krvi s bunkovými líniami CTC získanými od pacientov s malobunkovým karcinómom pľúc. Zistili, že CTC boli schopné indukovať diferenciáciu monocytov na TAM, ktoré vylučujú množstvo mediátorov , ako je osteopontín, MMP9, chitináza -3-1 a faktor krvných doštičiek, aby podporili ďalší nábor, migráciu a inváziu leukocytov149,150 . V ďalšej štúdii kolorektálneho karcinómu je spätná väzba medzi TAM a rakovinovými bunkami nevyhnutná pre program EMT CTC a intravazáciu do krvného obehu. Mechanicky IL6 odvodený z TAM reguluje invazívnosť prostredníctvom dráhy STAT3/miR-506-3p/FoxQ1, čo zase zvyšuje expresiu CCL2 nádorových buniek edukovaných TAM, čím pomáha získavať makrofágy151 . Zdá sa, že TAM podporujú CTC získavanie mechanickej priľnavosti a odolnosti, čím im pomáhajú vytvárať ochranné bunkové zhluky a poskytujú odolnosť voči šmykovému namáhaniu 152 . Fúzia makrofágov a nádorových buniek by mohla byť potenciálnym mechanizmom imunitného úniku a invázie. Ukázalo sa , že tieto hybridy makrofágov a nádorových buniek majú makrofágové fenotypy podobné M2 (CD163), ako aj epitelové markery (EpCAM) 153,154 a boli izolované z krvi pacientov s viacerými rakovinami, ako je PDAC155 , melanóm154 , rakoviny prsníka, vaječníkov a kolorekta 156 . Okrem toho, keď sa transplantovali myšiam, rozšírili sa široko a vytvorili lézie vo vzdialených tkanivách 154 , 155 . Nedávna štúdia Gasta a kol. odhalili, že fúzne hybridy môžu zvýšiť heterogenitu nádoru a metastatické správanie, čo ďalej koreluje so štádiom ochorenia a celkovým prežitím u niekoľkých druhov rakoviny 157 . Okrem toho väčšie hybridné veľkosti boli tiež spojené s horším prežitím u pacientov s nemalobunkovým karcinómom pľúc 158 . Pochopenie mechanizmu priamej interakcie a molekulárnej fúzie medzi CTC a makrofágmi má veľký význam pre identifikáciu terapeutických cieľov.
Interakcia CTC s krvnými doštičkami
Metastáza a progresia rakoviny sú výrazne ovplyvnené náborom a aktiváciou krvných doštičiek, ktoré podporujú prežitie CTC, ako aj ich výsev a rast na sekundárnych miestach 159 , 160 . Krvné doštičky sa môžu viazať a vytvárať agregáty s CTC v krvnom obehu a CTC rozširujú tvorbu agregácie uvoľňovaním protrombotických a prokoagulačných mikročastíc alebo expresiou tkanivového faktora 161,162 . Zistilo sa , že mediátory uvoľňujúce krvné doštičky, ako je TGF-p, urýchľujú EMT v CTC a podporujú inváziu a metastázy163,164 . Xiong a kol. nedávno zistili, že expresia proteínu tepelného šoku 47 bola indukovaná počas EMT, čo zvýšilo interakciu rakovinových buniek a krvných doštičiek prostredníctvom jeho závislej sekrécie kolagénu v bunkách rakoviny prsníka 165 . Je zaujímavé, že sa predpokladá, že krvné doštičky chránia CTC proti mechanickému namáhaniu 166 a vyvolávajú rezistenciu voči anoikis, ktorá je sprostredkovaná aktiváciou dráhy YAP1 167 . Okrem toho krvné doštičky podporujú únik CTC z útoku NK buniek prostredníctvom rôznych mechanizmov vrátane (1) agregátov krvných doštičiek, ktoré vytvárajú povrchové tienenie na obranu cytolyzačného účinku NK buniek; 168 (2) normálny MHC-I odvodený z krvných doštičiek, ktoré sú prenesené na povrch nádorovej bunky, čím bránia identifikácii NK buniek; 169 (3) downregulácia prirodzenej zabíjačskej skupiny 2, člena D (NKG2D) v NK bunkách TGF-β odvodeným od krvných doštičiek, ako aj uvoľňovanie ligandov NKG2D sprostredkované krvnými doštičkami, ktoré prispievajú k zhoršenej protinádorovej cytotoxicite; 170 , 171 a (4) glukokortikoidom odvodený ligand príbuzný TNF odvodený od krvných doštičiek, ktorý aktivuje GITR v NK bunkách a znižuje ich cytotoxicitu172 . Okrem toho NK bunky a krvné doštičky môžu tiež interferovať s neutrofilmi, T bunkami a makrofágmi a modulovať ich imunitnú funkciu173,174,175 . Okrem ochrany CTC v krvnom obehu sa krvné doštičky podieľajú aj na adhézii endotelových buniek. Prichytenie krvných doštičiek a CTC je sprostredkované receptormi adhézie krvných doštičiek, ako je integrín aIIbp3 a P-selektín, čím sa podporuje pevná priľnavosť CTC k stene endotelu 176 , 177 , 178 . Okrem toho krvné doštičky aktivované nádorovými bunkami uvoľňujú ATP z hustých granúl, čo potom indukuje aktiváciu endotelového receptora P2Y2 a umožňuje transendotelovú migráciu nádorových buniek zvýšením permeability179. Jedna štúdia tiež odhalila, že súhra medzi integrínom a6p1 na krvných doštičkách a jeho receptorom, dezintegrínom a metaloproteázou 9 na CTC, je nevyhnutná pre proces extravazácie rakovinových buniek180 . Krvné doštičky by tiež mohli zvýšiť vaskulárnu permeabilitu, aby pomohli extravazácii nádorových buniek. Napríklad predklinický model pľúcnych metastáz ukázal, že CD97 spojený s nádorovými bunkami, receptor spojený s G proteínom, môže iniciovať aktiváciu krvných doštičiek, čo vedie k sekrécii granúl, vrátane uvoľňovania ATP aj kyseliny lyzofosfatidovej181 . Podobne sa zistilo, že súhra medzi doštičkovo špecifickým receptorovým glykoproteínom VI a jeho ligandom galektínom-3 exprimovaným na bunkách rakoviny hrubého čreva a prsníka podporuje aktiváciu krvných doštičiek a sekréciu ATP182 . V dôsledku toho tieto sekrécie krvných doštičiek podporujú proces nádorových metastáz reguláciou vaskulárnej permeability. Nedávno Xu a spol. zistili, že Ptx@AlbSNO môže blokovať funkcie krvných doštičiek špecifické pre nádor na potlačenie EMT nádoru, ako aj na zabránenie adhézie krvných doštičiek okolo CTC. Ptx@AlbSNO môže tiež inhibovať sekréciu TGF-β a zvýšiť intratumorálnu infiltráciu imunitných buniek, aby sa zvrátil imunosupresívny TME, čím sa potláčajú vzdialené metastázy183 . Celkovo vzaté, úzky a komplexný presluch medzi CTC a krvnými doštičkami môže zahŕňať odlišné varianty molekúl a signálne dráhy a môže predstavovať sľubnú protinádorovú stratégiu, ktorá je obzvlášť atraktívna na liečbu niekoľkých druhov rakoviny.
Interakcia CTC s MDSC
MDSC sú heterogénnou podskupinou myeloidných buniek charakterizovaných imunosupresívnymi vlastnosťami, ktoré tiež podporujú metastatické šírenie. Podľa štandardného protokolu na izoláciu ľudských MDSC Cassetta et al. zistili, že polymorfonukleárne (PMN)-MDSC boli významne rozšírené medzi väčšinou typov rakoviny okrem melanómu v porovnaní s infekciou a zápalom184 . Predpokladá sa, že klastre CTC-MDSC sa vyhýbajú imunitnému dohľadu nad odpoveďou T buniek185 . Pokles cirkulujúcich MDSC bol skutočne spojený so zvýšením aktivovaných OX40+PD-1- T buniek u pacientov s difúznym veľkobunkovým B- lymfómom186 . Okrem toho Sprouse a kol. zistili, že in vitro kokultivácia CTC odvodených od pacientov s melanómom a rakovinou prsníka a PMN-MDSC zvýšila aktiváciu Notch v CTC prostredníctvom priamej interakcie medzi Jagged1 (ligandy Notch1) exprimovaným na MDSC a receptorom Notch1 exprimovaným na CTC. Zvýšená produkcia produkcie reaktívnych foriem kyslíka v MDSC by mohla zvýšiť expresiu receptora Notch1, čím by sa podporila proliferácia CTC187 . Potenciálne mechanizmy, ktoré sú základom súhry medzi CTC a MDSC, sa ešte musia určiť.
Interakcia CTC s modelmi CAF
CAF sú jednou z najrozšírenejších zložiek v TME a zohrávajú významnú úlohu pri iniciácii nádoru, angiogenéze, metastázovaní a rezistencii voči liekom188 . Mechanicky CAF remodelujú štruktúru extracelulárnej matrice, ktorá umožňuje nádorovým bunkám preniknúť cez strómu a komunikovať s rakovinovými bunkami vylučovaním rastových faktorov, chemokínov a cytokínov 189 . Málo sa však vie o súhre medzi modelmi CAF a CTC. Duda a spol. najprv demonštrovali, že CTC môžu prenášať CAF z primárneho nádoru do metastatického miesta na myšacích modeloch metastáz rakoviny pľúc190 . Tieto CAF odvodené od hostiteľa priamo zvyšujú prežitie nádorových buniek a podporujú tvorbu metastáz, zatiaľ čo vyčerpanie CAF z pľúc významne znižuje počet makroskopických metastáz a predlžuje mieru prežitia u myší. Okrem toho môžu CAF chrániť CTC pred šmykovými silami tekutiny počas procesu šírenia 191 . V trojrozmernom kokultivačnom modeli sa zistilo, že CAF indukujú šmykovú odolnosť voči nádorovým bunkám prostaty prostredníctvom stabilného medzibunkového kontaktu, ako aj rozpustné faktory (ako sú CXCL5, CCL2 a CCL7), ktoré sú spojené s prežitím buniek, inváziou a EMT. Okrem experimentálnych modelov boli cirkulujúce CAF (identifikované koexpresiou FAP a α-SMA) detegované v periférnej krvi pacientov s metastatickým karcinómom prsníka, ale nie u pacientov v skorých štádiách192 a vykazujú vynikajúcu presnosť v metastázach. diagnóza (AUC–ROC, 0,975), keď bola izolovaná pomocou novej akustickej mikrostreamingovej platformy193 .
Technológie na obohacovanie a izoláciu CTC
V posledných rokoch bolo navrhnutých mnoho metód na zachytenie CTC. Kvôli extrémne malému podielu CTC v krvi pacientov je stále veľkou výzvou presne izolovať CTC z mnohých krvných buniek a najmä vynájsť použiteľné metódy, ktoré dokážu efektívne odhaliť životaschopné CTC pre následnú hĺbkovú analýzu. Tu budeme diskutovať o vývoji technológií súvisiacich s CTC za posledné dve desaťročia, pretože zaznamenali obrovský rast. Zdôrazníme najinovatívnejšie metódy spojené s materiálmi nanometrov alebo novými mikrofluidnými čipmi v nádeji, že poskytneme užitočný rámec technológií súvisiacich s CTC.
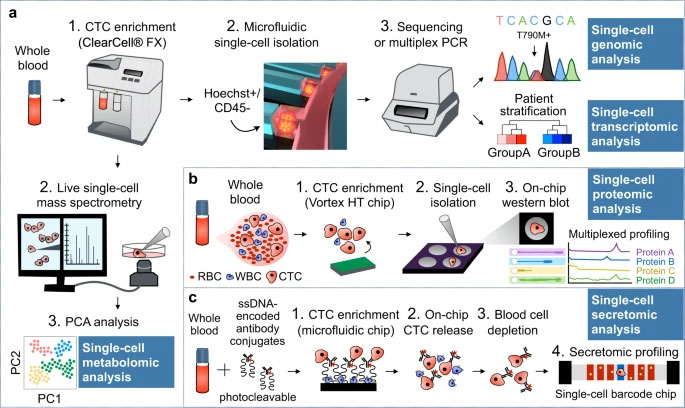
Vo všeobecnosti existujú tri základné stratégie technológií CTC194 , ktoré zahŕňajú (1) zachytávanie a obohacovanie, (2) detekciu a identifikáciu a (3) uvoľnenie. Prvá stratégia zachytávania a obohatenia zahŕňa špecifickú interakciu medzi CTC a materiálmi prostredníctvom fyzikálnych interakcií alebo interakcií protilátka-antigén. Druhá stratégia detekcie, ktorá znamená identifikáciu CTC, sa týka rôznych metód, ako je fluorescenčná mikroskopia, fluorescenčná spektrofotometria, prietoková cytometria, Ramanov rozptyl so zosilneným povrchom alebo elektrická impedancia. V poslednej stratégii sa uvoľnené CTC používajú hlavne na následnú analýzu, ako je genomika, transkriptomika, proteomika a kultúra CTC.
Klasické technológie súvisiace s CTC založené na fyzikálnych vlastnostiach
Fyzická separačná metóda obohatenia CTC je založená na rozdieloch medzi CTC a krvnými bunkami vo veľkosti, hustote, deformovateľnosti a elektrických vlastnostiach. Systém 195 izolácie podľa veľkosti epitelových nádorových buniek môže filtrovať vzorky krvi cez polykarbonátovú membránu typu TRACK-ETCH s priemerom 8 μm, ale má nízku účinnosť. Vylepšená metóda, ktorá pozostáva zo systému regulácie tlaku, pružného mikropružinového zariadenia 196 , dosahuje účinnosť záchytu 90 % s detekciou CTC v 76 % vzoriek. Existujú však rôzne trendy v počte CTC pozorované z rôznych vzoriek, takže táto metóda nie je spoľahlivá pre široké použitie. CTC možno triediť aj pomocou systému Oncoquick 197 , techniky závislej od hustoty, ktorá umožňuje filtráciu červených krviniek a bielych krviniek, alebo pomocou Apostream 198 , ktorý využíva techniky dielektrickej elektroforézy v mikrofluidnej komore na zachytenie CTC. Tieto systémy vyžadujú veľký objem krvi a nemôžu zbierať CTC podobnej veľkosti ako WBC, čo sú ich hlavné obmedzenia. Celkovo sú metódy založené na fyzikálnych vlastnostiach všeobecne neefektívne, majú nízku čistotu a nedostatočnú špecifickosť, hoci vitalita je dobrá a náklady sú relatívne lacné.
Klasické technológie súvisiace s CTC založené na biologických vlastnostiach
Technológia založená na biologických vlastnostiach je ďalšou dôležitou metódou detekcie CTC. Na základe interakcie protilátka-antigén sú CTC zvyčajne pozitívne obohatené pomocou epitelových (EpCAM) a mezenchymálnych (vimentín) markerov, ako aj negatívne obohatené použitím CD45 na vyčerpanie nežiaducich leukocytov199 . Techniky závislé od EpCAM sú najčastejšie používané výskumníkmi. Systém CellSearch 200 , jediné zariadenie schválené FDA na klinické použitie, využíva feromagnetické guľôčky potiahnuté protilátkou EpCAM na obohatenie CK + /CD45-/DAPI + CTC a odstránenie CK-/CD45 + /DAPI + WBC. Avšak CTC silne priľnú k povrchu zariadenia v metódach založených na interakcii protilátok, čo sťažuje ich uvoľnenie. Tento nedostatok môže byť vyriešený v inom EpCAM závislom systéme MagsWeeper 201 , ktorý používa magnetickú tyč na obohatenie CTC a elimináciu buniek neviazaných na magnetické guľôčky, čo umožňuje uvoľnenie CTC pre nasledujúcu biochemickú analýzu. Canpatrol TM 202 je ďalším predstaviteľom EpCAM-dependentnej techniky, ktorá poskytuje morfologickú, cytologickú a genetickú charakterizáciu jednotlivých CTC. Stručne povedané, techniky založené na EpCAM sú široko používané. Avšak, pretože povrchový antigén CTC má vysokú heterogenitu, CTC, ktoré majú nízku expresiu EpCAM, nemusia byť obohatené, čo spôsobuje nepresné výsledky, zatiaľ čo metódy založené na fyzikálnych vlastnostiach nemajú toto obmedzenie. Pozornosť výskumníkov si preto postupne získalo kombinovanie výhod rôznych technológií alebo hľadanie CTC s vysokou citlivosťou a špecifickými nádorovými markermi.
Nedávno, s vývojom mikrofluidných čipov, nanomateriálov a sekvencovania novej generácie, majú výskumníci veľa pokročilých technológií na stimuláciu pokroku v technológiách súvisiacich s CTC. Dôležité je, že výskumníci sa snažia dosiahnuť vyššiu úroveň technológií súvisiacich s CTC v niekoľkých kľúčových parametroch: výťažok, čistota, pomer obohatenia, priepustnosť, životaschopnosť, citlivosť, špecifickosť, rýchlosť uvoľňovania, dostupnosť pre ďalšiu analýzu a jednoduchosť prevádzky zariadenia).
Najnovšie technológie súvisiace s CTC: techniky založené na mikrofluidoch a nanotechnológiách
Okrem klasických technológií súvisiacich s CTC diskutovanými vyššie boli vyvinuté niektoré novšie technológie, ako sú techniky založené na mikrofluidoch a nanotechnológiách. Mikrofluidické prístupy k triedeniu buniek využívajú „vnútorné“ (napr. dynamické sily tekutiny) oproti „vonkajším“ vonkajším silám (napr. magnetické, elektrické pole, akustické a optické sily) na oddelenie buniek a potom vyberte cieľové bunky zo vzorky heterogénne bunky prostredníctvom rôznych fyzikálnych a biologických vlastností 203 . CTC čip je silikónová mikrofluidná platforma, na ktorej sú CTC zachytené na sklíčkach potiahnutých molekulárnym markerom. CTC čip 204 dokáže oddeliť životaschopné CTC z plnej krvi bez predbežného označovania alebo spracovania vzoriek, čo vedie k zvýšenej bunkovej aktivite a čistote separácie. Upravená platforma založená na čipe využívajúca zlaté nanočastice na čipe rybej kosti (NP- HB CTC-Chip 205 ) ľahko oddeľuje životaschopné CTC a bezpečne uvoľňuje bunky na ďalšiu analýzu pomocou reakcie chemickej výmeny ligandov s nanočasticami zlata na čipe rybej kosti. Okrem toho má monolitický CTC-iChip 206 vysokoúčinnú depléciu WBC a umožňuje charakterizáciu CTC s epiteliálnymi a mezenchymálnymi charakteristikami. Hoci tieto mikrofluidné čipy výrazne prispeli k vývoju detekcie CTC (tj zlepšenej účinnosti zachytávania, životaschopnosti a vyčerpania bielych krviniek), nie sú široko používané na klinické použitie kvôli obmedzeniam, medzi ktoré patrí dlhý čas nastavenia, vysoké počiatočné náklady, objemné prístrojové vybavenie a obmedzená schopnosť vykonávať jednobunkovú molekulárnu analýzu.
V snahe zachytiť CTC automatizovaným spôsobom (tabuľka 2 ), Zhang et al. úspešne triedili bunky MCF-7 z 5 ml objemu zriedenej krvi do 23 m s mierou obnovy 85 % 207 . Ešte pozoruhodnejšie je, že Jia a kol. vyvinuli menej nákladný samoriadiaci mikrodutinový čip na dosiahnutie načítania buniek, lýzy, izotermického zosilnenia a čítania signálu na jedinom čipe 208 . Tento nový čip dokáže vykonávať genetickú analýzu na úrovni jednotlivých buniek, má veľký potenciál v personalizovanej terapii a monitorovaní účinnosti. Okrem toho ďalší automatizovaný a integrovaný mikrofluidný systém navrhnutý Wangom a kol. sa uvádza, že dosiahne zachytenie a identifikáciu CTC do 90 m. S výhodami automatizácie, stability, hospodárnosti a užívateľsky prívetivej prevádzky poskytuje tento systém široké vyhliadky na skríning a prognózu rakoviny, najmä pri HCC 209 . Okrem toho Lee a kol. vynašiel integrovaný systém na báze mikrofluidov na dosiahnutie súčasnej izolácie na čipe a charakterizáciu cirkulujúcich nádorov s využitím rozdielov v gradiente magnetického poľa a imunitnej fluorescencii. Okrem toho tento nový systém dokáže na čipe rozlíšiť osem rôznych podtypov heterogénnych CTC, čo vedie k diagnóze a prognóze rakoviny prsníka210 . Kombináciou mikrofluidnej technológie a techník molekulárneho profilovania in situ má čipová platforma On-chip Post-processing Enabling schopnosť vykonávať molekulárne analýzy jedného CTC z pacientov s metastatickým karcinómom prsníka a metastatickým karcinómom pankreasu bez akýchkoľvek procesov mimo čipu, čo naznačuje jeho potenciálna implementácia včasnej molekulárnej detekcie metastáz rakoviny 211 . Menej nákladné automatizované a integrované mikrofluidné systémy, ktoré umožňujú jednoduchú detekciu CTC a analýzu buniek, majú spolu veľkú klinickú hodnotu.
S pokrokom v oblasti nanomateriálov sa metódy založené na nanotechnológiách stávajú sľubnými nástrojmi na detekciu CTC v počiatočnom štádiu ochorenia a na monitorovanie vývoja rakoviny, ako aj zobrazovanie in vivo 212 . Nanomateriály majú veľký pomer povrchu k objemu a umožňujú izoláciu CTC pri vysokej špecifickosti a detekciu CTC pri vysokej citlivosti tým, že adsorbujú množstvo cieľových ligandov na naviazanie špecifických molekúl na rakovinové bunky. V súčasnosti štúdie uvádzajú mnohé typy nanomateriálov (tabuľka 2 ) na detekciu CTC, vrátane magnetických nanočastíc 213 , 214 , 215 , 216 , 217 , nanočastíc zlata 218 , 219 , 220 a kvantových , 22221 bodov 221 . Štúdie napríklad ukázali, že využitie magnetických nanočastíc214 funkcionalizovaných kyselinou trieslovou , magnetických nanohybridov CoFe2O4@Ag216 a magnetických nanočastíc na báze peptidov213 zvyšuje účinnosť zachytávania CTC u pacientov s rakovinou prsníka. Medzi nimi magnetické nanočastice na báze peptidov dokážu rozlíšiť epitelové a mezenchymálne podskupiny CTC a umožňujú analýzu na úrovni jednej bunky, ktorej detekčné účinky sú podporované magnetickými nanočasticami a integrovanými systémami na báze mikrofluidov 210 . Pokiaľ ide o nanočastice zlata, došlo k významnému vývoju. Napríklad cytosenzor navrhnutý Yangom a kol. 224 vykazovali vynikajúci analytický výkon so širokým lineárnym rozsahom, uspokojivým uvoľňovaním CTC (93,7–97,4 %) a dobrou životaschopnosťou buniek. Liu a kol. uviedli, že nanovrstvy čierneho fosforu modifikované nanočasticami zlata zlepšili stabilitu pri detekcii CTC218 . Okrem toho kombinácia mikrofluidného systému a nanočastíc zlata predstavuje širšiu škálu aplikácií. Wang a kol. syntetizovať medzifázový povlak oxidu zinočnatého s nanoštruktúrou na povrchu mikroguľôčok, čo zväčšuje špecifický povrch a tým vedie k zlepšenej účinnosti zachytávania CTC225 . Navyše, využitie viacfarebných magnetických povrchovo vylepšených Ramanových rozptylových nanotagov a čipovej imunomagnetickej separácie by mohlo kvantitatívne a simultánne detekovať štyri rôzne povrchové proteínové markery na jednotlivých nádorových bunkách, čím by sa uľahčilo oddelenie CTC subpopulácií 217 .
Hoci techniky založené na nanotechnológiách môžu poskytnúť široké vyhliadky na výskum CTC v rôznych nádoroch nákladovo efektívnym a jednoduchým spôsobom, existujú obmedzenia a výzvy. Po prvé, mnohé faktory (napr. väzba nanočasticových sond, agregácia) môžu ovplyvniť detekciu založenú na nanočasticiach, čo vedie k zníženiu spoľahlivosti a reprodukovateľnosti. Po druhé, väčšina testov na báze nanočastíc sa pripravuje na akademické štúdie a stále sú nereálne pre široko klinický preklad. Po tretie, existuje možná toxicita nanočastíc.
V ére presnej medicíny má analýza CTC veľkú klinickú hodnotu. Ak majú pracovníci robiť svoju prácu dobre, nástroje sa musia najskôr nabrúsiť. Preto sú technológie súvisiace s CTC základným základom pre aplikáciu CTC v presnej medicíne. Tu sme preskúmali predchádzajúce technológie súvisiace s CTC založené na fyzikálnych a biologických vlastnostiach a najnovší vývoj techník spojených s prístupmi založenými na mikrofluidoch a nanočasticiach. Aj keď medzi rôznymi metódami existujú silné a slabé stránky, veríme, že efektívna kombinácia týchto techník môže byť prínosom pre výskum CTC mnohými spôsobmi, najmä pokiaľ ide o hĺbkovú analýzu a možnosti v klinických aplikáciách.
Klinické aplikácie CTC
Klinicky sa CTC teraz používajú ako náhradné biomarkery pre mnohé solídne rakoviny. Uskutočnilo sa množstvo štúdií, najmä pri rakovine prsníka, rakovine prostaty, rakovine pľúc, rakovine pečene, rakovine pankreasu, rakovine žalúdka a melanóme. Hoci klinické usmernenia nezahŕňali klinické použitie CTC, okrem zaradenia CTC do klasifikácie nádorov cM0 (t. j. žiadne klinické prejavy zjavných metastáz, ale detekcia nádorových buniek v krvi), mnohé štúdie predpovedali veľký potenciál CTC v klinických aplikáciách. V tejto časti predstavíme najmä úlohu CTC ako biomarkerov na diagnostiku, prognostiku a monitorovanie terapie pri rôznych rakovinách (obr. 4 ).
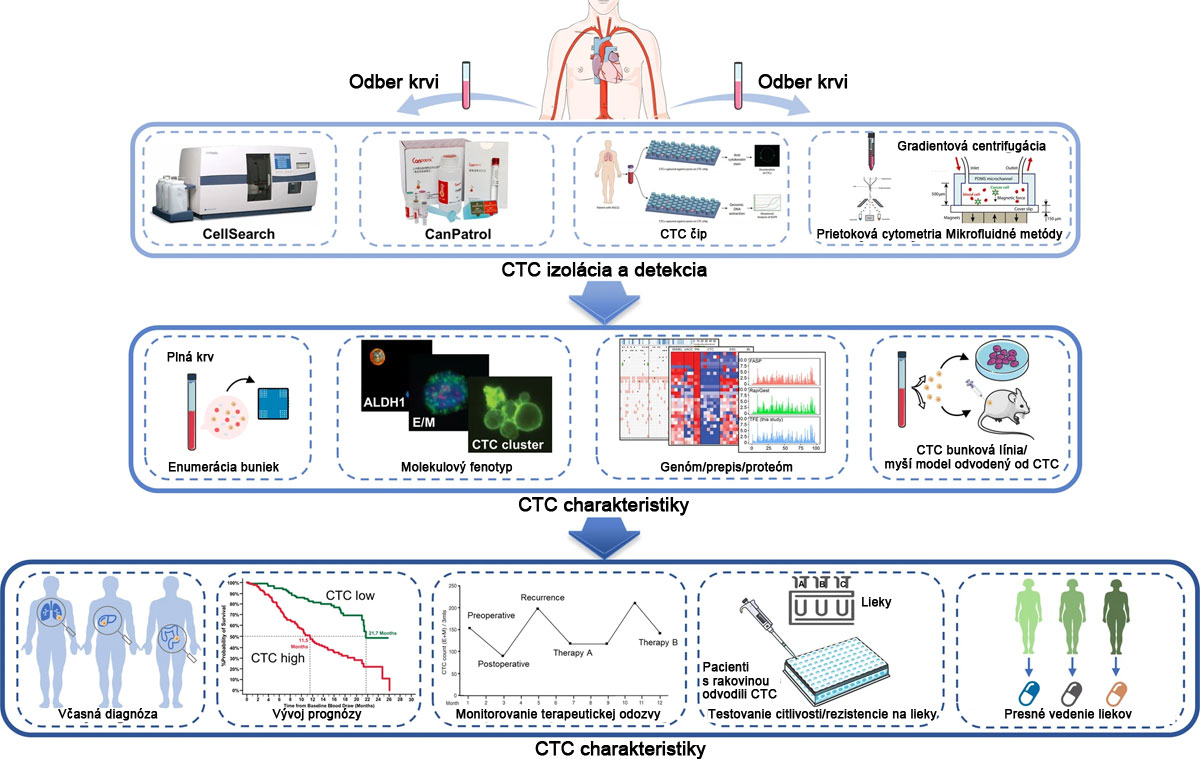
Včasná diagnostika rakoviny
Ako neinvazívna metóda je detekcia CTC atraktívna pri diagnostike rakoviny. Štúdie CTC používané na včasnú diagnostiku rakoviny v posledných troch rokoch sú uvedené v tabuľke 3 . Nádorová lézia už má viac ako 109 nádorových buniek v čase, keď sú detekovateľné u pacientov pomocou súčasných zobrazovacích postupov 15 , ako je počítačová tomografia, magnetická rezonancia a pozitrónová emisná tomografia. Čo najskoršia diagnostika rakoviny, najmä v prípade rýchlo progredujúcej rakoviny, je najlepší spôsob, ako ich poraziť. Štúdie zistili, že CTC korelujú so štádiom nádoru, ale klinická užitočnosť CTC pri detekcii rakoviny alebo dokonca pri včasnej diagnostike rakoviny je stále predmetom diskusie. CTC sa považujú za náhradný marker metastatickej aktivity, ale to, či sa metastatické šírenie CTC u pacientov vyskytuje včas počas tvorby nádoru, je stále kontroverzné. Na myších modeloch sa však zistila skorá diseminačná metastáza v karcinogenéze prsníka 226 , 227 a pankreasu 228 , 229 , čo naznačuje, že cirkulácia CTC je pravdepodobne veľmi skorým javom v progresii rakoviny. V štúdii Barrière et al. 230 boli CTC detegované u 41 % pacientov v štádiu T1 a 47 % pacientov s rakovinou prsníka s negatívnymi axilárnymi lymfatickými uzlinami, pričom obe sú v počiatočnom štádiu rakoviny prsníka. V štúdii Thery et al. 231 miera pozitivity CTC bola 21 % a 24 % pri rakovine prsníka s negatívnymi lymfatickými uzlinami a 24 % s pozitívnou rakovinou prsníka. Na základe tejto hypotézy môžu byť CTC detegované skôr, než je primárny nádor viditeľný na zobrazovacích štúdiách, zatiaľ čo najväčšou výzvou aplikácie CTC pri včasnej diagnostike rakoviny je skutočne ich nedostatok a izolácia. Obmedzená citlivosť metód detekcie CTC bráni ich použitiu ako účinného biomarkera vo včasnej diagnostike rakoviny.
Tabuľka 3 Klinické aplikácie CTC za posledné tri roky (od roku 2019 do roku 2021)
Hodnotenie prognózy rakoviny
Prognostická hodnota CTC bola dôkladne študovaná. CellSearch je jediný klinicky používaný systém na detekciu CTC schválený FDA. Na základe systému CellSearch 46 , 232 , 233 , 234 , 235 , 236 , 237 , 238 , 239 , 240 , 241 , 242 , 243 , 244 , 245 , predstavujú nezávislý prognostický faktor Štúdie hodnotiace iné CTC detekčné systémy ako CanPatol, CTC-čip dosiahli podobné výsledky. Hlavným cieľom vyšetrovania je stanovenie CTC s hraničnou hodnotou ≥ 5 pre pozitivitu, ktorá zvyčajne naznačuje horšiu prognózu. Všeobecne sa predpokladá, že zvýšené počty CTC korelujú s vyššou pravdepodobnosťou metastáz a agresivity rakoviny. V metaanalýze 2239 pacientok s rakovinou prsníka vrátane 21 štúdií 246 mal počet CTC pred neoadjuvantnou chemoterapiou škodlivý a klesajúci vplyv na prežívanie pacientov a pacienti s jedným, dvoma, tromi až štyrmi a piatimi alebo viacerými CTC vykazovali HR. úmrtia (95 % CI) 1,09 (0,65–1,69), 2,63 (1,42–4,54), 3,83 (2,08–6,66) a 6,25 (4,34–9,09). Okrem toho, zvýšené východiskové hladiny CTC boli spojené s horším prežitím, prítomnosť zhlukov CTC často predpovedala zlú prognózu 247 , 248 , 249 a zvyšujúci sa počet CTC alebo nevyčistenie CTC počas liečby bolo tiež prognostickým faktorom horšieho prežitia234 , 250 , 251 . Mnohé štúdie zistili, že molekulárne fenotypy CTC majú silnú prognostickú hodnotu. EMT a stopka sú hlavné molekulárne fenotypy CTC študovaných klinicky. CTC s expresiou markerov súvisiacich s mezenchymálnymi 252 alebo kmeňovými 253 spojenými s horším prežitím. Expresia iných molekulárnych markerov, ako napríklad HER246 , CD47254 , PD-L1254 , má tiež prognostické dôsledky. Väčšina štúdií skúma prognostickú hodnotu CTC v jedinom časovom bode, zatiaľ čo je zaujímavé, že niektoré štúdie zohľadnili dynamiku CTC. Magbanua a kol. 237vyvinuli nový model latentnej zmesi na stratifikáciu skupín s podobnými vzormi trajektórie CTC počas liečebného cyklu a zistili, že analýza sériových CTC môže ďalej stratifikovať pacientov so zlou prognózou do odlišných prognostických podskupín. Dynamické zmeny CTC môžu pôsobiť ako náhradný biomarker prognózy počas dlhého priebehu progresie rakoviny. Vzhľadom na rýchly pokrok v dostupnosti a posilňovaní sekvenčných technológií na úrovni jednotlivých buniek môžeme očakávať, že v budúcnosti môžu genómové/transkripčné profily CTC slúžiť ako vynikajúci prognostický marker, ktorý bude predstavovať komplexnejšie a komplexnejšie biologické informácie. úzko súvisí s prognózou. Štúdie CTC na predpovedanie prognózy v posledných troch rokoch sú zhrnuté v tabuľke 3 .
Monitorovanie terapeutickej odpovede
V mnohých klinických štúdiách boli CTC použité ako užitočné biomarkery na monitorovanie odpovedí na liečbu rakoviny 234 , 255 , 256 , 257 , buď v kombinácii so zobrazovacími vyšetreniami, sérovými biomarkermi alebo samostatne. Výskumníci uprednostňujú zapojenie CTC do hodnotenia terapeutickej účinnosti vzhľadom na vyššiu citlivosť CTC ako v niektorých prípadoch zobrazovacie vyšetrenie 9 . Ako neinvazívna metóda môže detekcia CTC prispieť aj k tomu, aby sa zabránilo častému ožiareniu zo zobrazovacích štúdií počas hodnotenia odpovede na liečbu. Väčšina štúdií zistila, že pokles alebo klírens počtu CTC súvisel s dobrou terapeutickou odpoveďou, zatiaľ čo zvýšenie počtu CTC znamenalo opak 258 , 259 . Smernice RECIST (Response Evaluation Criteria in Solid Tumors) sú najčastejšie používaným štandardom na hodnotenie terapeutickej odpovede v prípade solídnych nádorov. V niektorých štúdiách však zmeny CTC po liečbe nekorelovali s odpoveďami RECIST u pacientov s rakovinou260 . Hodnotenie CTC v skutočnosti nebolo zahrnuté do usmernení RECIST. Niektoré technológie merania CTC boli nedávno vyvinuté na dosiahnutie genotypizácie pre CTC, ktoré môžu tiež odhaliť kľúčové génové mutácie, ako napríklad ER 39 , 49 , HER2 39 , 49 , EGFR 261 , KRAS 262 a TP53 263 , čím pomáhajú lekárom pri personalizácii liečby. a možnosti rezistencie v čase progresie nádoru. Štúdie využívajúce CTC na monitorovanie odpovede na liečbu v posledných troch rokoch sú zhrnuté v tabuľke 3 .
Objavil sa veľký potenciál CTC v klinickej aplikácii diagnostiky rakoviny, hoci klinicky je jeho použitie ako náhradného biomarkera na skríning rakoviny, monitorovanie liečby a predpovedanie prognóz stále obmedzené. Akonáhle dôjde k metastáze, je zvyčajne ťažké získať opakované biopsie metastatických lézií a rôzne metastázy sú heterogénne dokonca aj u tých istých pacientov. Testovanie CTC pomocou vzoriek periférnej krvi je pohodlné a môže byť reprezentatívnejšie pre znaky metastatických buniek, ktoré sú odvodené od rôznych metastatických lézií u pacientov. Napriek tomu stále chýbajú usmernenia pre klinické použitie CTC, ako je štandardizovaný test na detekciu CTC pre rôzne druhy rakoviny, kombinovaná diagnostická schéma s inými klinickými vyšetreniami a indikácie vhodných časových bodov na odber vzoriek krvi.
Diskusia
Štúdie skúmajúce CTC majú veľký potenciál odhaliť základné procesy metastáz, vrátane mechanizmov zapojených do extravazácie CTC z primárneho nádoru, ako CTC interagujú s krvnými bunkami, aby prežili v obehovom mikroprostredí, a ako CTC prenikajú do vzdialeného metastatického miesta. iniciovať nové lézie. Významné molekulárne vlastnosti CTC môžu výrazne prispieť k identifikácii cieľov pre antimetastatické terapie. Iba malá časť CTC môže nakoniec generovať metastázy, takže štúdie zamerané na tieto silne metastatické CTC môžu poskytnúť hlbší pohľad na terapeutické ciele súvisiace s CTC.
Objavili sa rôzne technológie na detekciu CTC, avšak citlivosť a špecifickosť týchto technológií je ešte potrebné ďalej zlepšovať. Technológia detekcie CTC založená na epiteliálnych markeroch, ako je systém CellSearch, otvorila novú éru pre analýzu CTC a klinické aplikácie, ale ich nevýhody rýchlo uznávajú a oceňujú výskumníci. EMT je kľúčovým znakom metastatických rakovinových buniek, čo naznačuje nedostatočnú účinnosť zachytávania technológie detekcie CTC založenej na epiteliálnych markeroch. Detekčné technológie založené na mezenchymálnych markeroch však môžu byť kontaminované aj inými ako CTC, ako sú fibroblasty spojené s nádorom a endotelové zhluky, ktoré vyvolávajú riziko falošnej pozitivity. Napriek tomu je zaujímavé, že nedávne štúdie uvádzajú, že tieto bunky odvodené od nerakovinových nádorov prezentované u pacientov s rakovinou sú tiež dôležitými náhradnými biomarkermi pre pacientov s rakovinou 264 . Molekulárne markery špecifické pre typ rakoviny pre CTC sú pravdepodobne ďalšou možnosťou, pretože CTC rôznych typov rakoviny majú rôzne molekulárne markery. Senzitivita a špecifickosť známych CTC markerov špecifických pre typ rakoviny však nie sú uspokojivé. Technológie detekcie CTC založené na fyzikálnych vlastnostiach majú tiež problém kontaminácie ne CTC, najmä v prípade tých, ktoré majú podobné fyzikálne vlastnosti ako CTC. Detekčné technológie CTC založené na mikrofluidoch a nanotechnológiách sa v posledných rokoch stali populárnymi, pričom účinnosť týchto technológií si stále vyžaduje ďalšie rozsiahle klinické overenie. Vysoká účinnosť detekcie buniek a schopnosť odstraňovania kontaminácie sú dve kľúčové silné stránky úspešnej technológie detekcie CTC, pričom na dosiahnutie týchto požiadaviek je naliehavo potrebná podstatná technická optimalizácia detekcie CTC.
Chýba komplexná charakteristika CTC. Obmedzené množstvo obsahu genómovej DNA, RNA a proteínov v CTC je prekážkou pri skúmaní ich vlastností genómu, transkriptómu, epigenómu a proteómu. Napriek tomu vznikajúce štúdie genómu a transkriptómu CTC nedávno profitovali z rýchlo sa vyvíjajúcej technológie jednobunkového sekvenovania, zatiaľ čo štúdie proteómov CTC sú stále nepolapiteľné kvôli veľmi obmedzeným technológiám na skúmanie proteómov na úrovni jednej bunky. Štúdium proteómu CTC je však bezprostredné, nielen preto, že môže poskytnúť obraz o biologickej charakterizácii CTC, ale aj preto, že môže pomôcť objaviť CTC špecifické membránové proteíny, ktoré môžu pomôcť optimalizovať detekciu CTC.
Pokiaľ ide o mikroprostredie solídneho nádoru, krvné mikroprostredie okolo CTC tiež zohráva významnú úlohu v prežívaní nádoru a inváznej kapacite. Poznatky o základných mechanizmoch prežitia CTC sú však stále obmedzené, pretože ide o zložitý proces, ktorý zahŕňa nielen šmykové sily a mechaniku tekutín, ale aj rozpustné faktory a extracelulárne vezikuly spojené s nádorom, ktoré tu nie sú podrobne uvedené. Ďalej zostáva potvrdiť, či sú zhluky CTC vhodnejšie na interakciu s inými zložkami krvi alebo na prispôsobenie sa šmykovým silám ako jednotlivé migrujúce CTC. Ak sa skombinujeme so špecifickými biomarkermi na strategickú detekciu CTC a interakciu CTC s pridruženými periférnymi krvnými bunkami, mohli by sme zlepšiť klinickú praktickosť a monitorovaciu silu CTC získaním komplexnejších informácií o nádorovej záťaži a imunitnom stave pacientov.
Hoci CTC preukázali počiatočný sľub v klinických aplikáciách, je potrebné prekonať mnohé výzvy, kým sa analýza CTC bude môcť široko aplikovať na klinike. Dnes klinická aplikácia CTC závisí hlavne od analýzy počítania buniek CTC a molekulárnych fenotypov. Komplexnejšia charakterizácia CTC na základe ich genómu, transkriptómu a proteómu s vysokovýkonným sekvenovaním bude ďalším prínosom pre klinickú aplikáciu, ale tiež zvýši zložitosť a náročnosť analýzy údajov. CTC budú v budúcnosti kľúčovou zložkou „presnej medicíny“, pretože fenotypová, genotypová a funkčná charakterizácia môže poskytnúť príležitosť na štúdium citlivosti na lieky, ktorá súvisí s metastázami. Analýza genómu a transkriptómu CTC môže odhaliť potenciálne ciele liečiv. Životaschopné CTC na testovanie citlivosti/rezistencie na liečivo počas terapeutického kurzu môžu viesť k presnej medikácii. Kultivácia CTC je však veľmi náročná: (1) sú dostupné obmedzené metódy na izoláciu životaschopných CTC, ktoré tiež poskytujú nízky počet CTC a (2) je ťažké napodobniť priaznivé obehové mikroprostredie na prežitie CTC. Boli stanovené veľmi obmedzené bunkové línie odvodené od CTC od pacientov s rakovinou. Bude potrebná optimalizácia kultivačných podmienok CTC.
Okrem toho sú vo vzorkách tekutej biopsie prítomné CTC, cirkulujúca nádorová DNA (ctDNA) a exozómy. Na dosiahnutie presnejšej diagnózy je potrebné preskúmať výhody a nevýhody každého substrátu prítomného v tekutých biopsiách a ako ich lepšie začleniť do klinickej aplikácie. Medzi metódami tekutej biopsie majú CTC obrovské výhody, pretože izolované CTC môžu byť životaschopné, čo môže optimalizovať explantáty odvodené od CTC alebo trojrozmerné organoidné kultúry na funkčné testovanie alebo testy na skríning liekov. Štúdium CTC je atraktívne a detekcia CTC sa pravdepodobne v budúcnosti môže stať základnou súčasťou liečby rakoviny. Keď sa obraz stáva jasnejším, sme si plne istí sľubným potenciálom CTC.
Referencie
- Sethi, N. & Kang, Y. Odhalenie zložitosti molekulárneho porozumenia metastáz a cielených terapií. Nat. Rev. Cancer 11 , 735-748 (2011).
Článok CAS PubMed Študovňa Google
- Lambert, AW, Pattabiraman, DR & Weinberg, RA Objavujúce sa biologické princípy metastáz. Cell 168 , 670-691 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Paget, S. Distribúcia sekundárnych rastov pri rakovine prsníka. 1889. Cancer Metastasis Rev. 8 , 98-101 (1989).
- Jones, S. a kol. Porovnávacie sekvenovanie lézií poskytuje pohľad na vývoj nádoru. Proc. Natl Acad. Sci. USA 105 , 4283-4288 (2008).
Článok CAS PubMed PubMed Central Študovňa Google
- Ley, TJ a kol. Sekvenovanie DNA cytogeneticky normálneho genómu akútnej myeloidnej leukémie. Nature 456 , 66-72 (2008).
Článok CAS PubMed PubMed Central Študovňa Google
- Hosseini, H. a kol. Včasné šírenie semien metastázuje pri rakovine prsníka. Príroda 540 , 552–558 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Chen, S. a kol. Skríning CRISPR v celom genóme v myšom modeli rastu nádoru a metastáz. Cell 160 , 1246-1260 (2015).
Článok CAS PubMed PubMed Central Študovňa Google
- Navin, N. a kol. Vývoj nádoru odvodený od jednobunkového sekvenovania. Nature 472 , 90-94 (2011).
Článok CAS PubMed PubMed Central Študovňa Google
- Yu, M. a kol. Cirkulujúce bunky nádoru prsníka vykazujú dynamické zmeny v epiteliálnom a mezenchymálnom zložení. Science 339 , 580-584 (2013).
Článok CAS PubMed PubMed Central Študovňa Google
- Peinado, H. a kol. Melanómové exozómy vzdelávajú progenitorové bunky kostnej drene smerom k prometastatickému fenotypu prostredníctvom MET. Nat. Med. 18 , 883-891 (2012).
Článok CAS PubMed PubMed Central Študovňa Google
- Aceto, N. a kol. Zhluky cirkulujúcich nádorových buniek sú oligoklonálnymi prekurzormi metastáz rakoviny prsníka. Cell 158 , 1110-1122 (2014).
Článok CAS PubMed PubMed Central Študovňa Google
- Quail, DF & Joyce, JA Mikroenvironmentálna regulácia progresie nádoru a metastáz. Nat. Med. 19 , 1423-1437 (2013).
Článok CAS PubMed PubMed Central Študovňa Google
- Ashworth, TR Prípad rakoviny, pri ktorej boli po smrti v krvi pozorované bunky podobné tým v nádoroch. Austrália. Med. J. 14 , 146-149 (1869).
- Pantel, K. & Speicher, MR Biológia cirkulujúcich nádorových buniek. Oncogene 35 , 1216-1224 (2016).
Článok CAS PubMed Študovňa Google
- Alix-Panabieres, C. & Pantel, K. Výzvy vo výskume cirkulujúcich nádorových buniek. Nat. Rev. Cancer 14 , 623-631 (2014).
Článok CAS PubMed Študovňa Google
- Harper, KL a kol. Mechanizmus skorého šírenia a metastáz pri Her2+ rakovine prsníka. Nature 540 , 588–592 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Hosseini, H. a kol. Včasné šírenie semien metastázuje pri rakovine prsníka. Príroda 540 , 552–558 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Lianidou, ES & Markou, A. Cirkulujúce nádorové bunky pri rakovine prsníka: detekčné systémy, molekulárna charakterizácia a budúce výzvy. Clin. Chem. 57 , 1242-1255 (2011).
Článok CAS PubMed Študovňa Google
- Thanh Huong, P. a kol. Vznikajúca úloha cirkulujúcich nádorových buniek pri rakovine žalúdka. Cancers 12 , 695-716 (2020).
Článok PubMed Central Študovňa Google
- Gires, O., Pan, M., Schinke, H., Canis, M. & Baeuerle, PA Expresia a funkcia adhéznej molekuly epitelových buniek EpCAM: kde sme po 40 rokoch? Cancer Metastasis Rev. 39 , 969-987 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Popovič, D., Vučič, D. & Dikič, I. Ubikvitinácia v patogenéze a liečbe chorôb. Nat. Med. 20 , 1242-1253 (2014).
Článok CAS PubMed Študovňa Google
- Criscitiello, C., Sotiriou, C. & Ignatiadis, M. Cirkulujúce nádorové bunky a objavujúce sa krvné biomarkery pri rakovine prsníka. Curr. Opin. Oncol. 22 , 552-558 (2010).
Článok CAS PubMed Študovňa Google
- Gorin, MA a kol. Cirkulujúce nádorové bunky ako biomarkery rakoviny prostaty, močového mechúra a obličiek. Nat. Rev. Urol. 14 , 90-97 (2017).
Článok CAS PubMed Študovňa Google
- Varillas, JI a kol. Mikrofluidná izolácia cirkulujúcich nádorových buniek a rakovinových kmeňových buniek od pacientov s pankreatickým duktálnym adenokarcinómom. Theranostics 9 , 1417–1425 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Marcuello, M. a kol. Cirkulujúce biomarkery na včasnú detekciu a klinickú liečbu kolorektálneho karcinómu. Mol. Asp. Med 69 , 107-122 (2019).
- Xia, W. a kol. In vivo súčasná identifikácia cirkulujúcich nádorových buniek hepatocelulárneho karcinómu pomocou dvojito cielených magneticko-fluorescenčných nanoguľôčok. Nano Lett. 21 , 634-641 (2021).
Článok CAS PubMed Študovňa Google
- Ye, Q., Ling, S., Zheng, S. & Xu, X. Kvapalná biopsia pri hepatocelulárnom karcinóme: cirkulujúce nádorové bunky a cirkulujúca nádorová DNA. Mol. rakovina 18 , 114 (2019).
Článok PubMed PubMed Central Študovňa Google
- Gall, TMH, Belete, S., Khanderia, E., Frampton, AE & Jiao, LR Cirkulujúce nádorové bunky a bezbunková DNA v pankreatickom duktálnom adenokarcinóme. Am. J. Pathol. 189 , 71 – 81 (2019).
Článok CAS PubMed Študovňa Google
- Eslami, SZ, Cortes-Hernandez, LE & Alix-Panabieres, C. Adhézna molekula epitelových buniek: kotva na izoláciu klinicky relevantných cirkulujúcich nádorových buniek. Cells 9 , 1836-1852 (2020).
- Wang, J. a kol. Izolácia bez označenia a detekcia mRNA cirkulujúcich nádorových buniek od pacientov s metastatickým karcinómom pľúc na diagnostiku ochorenia a monitorovanie terapeutickej účinnosti. Anal. Chem. 87 , 11893-11900 (2015).
Článok CAS PubMed Študovňa Google
- Wang, ZL a kol. Vysokoúčinná izolácia a rýchla identifikácia heterogénnych cirkulujúcich nádorových buniek (CTCS) pomocou fluorescenčných magnetických nanočastíc modifikovaných duálnymi protilátkami. ACS Appl. Mater. Rozhranie 11 , 39586–39593 (2019).
- Wang, Z. a kol. Magnetické nanočastice potiahnuté hydrogélom na selektívnu izoláciu a obnovu cirkulujúcich nádorových buniek. J. Mater. Chem. B 9 , 677-682 (2021).
Článok CAS PubMed Študovňa Google
- Reduzzi, C. a kol. Nová subpopulácia cirkulujúcich nádorových buniek na monitorovanie liečby a molekulárnu charakterizáciu pri rakovine žlčových ciest. Int J. Cancer 146 , 3495-3503 (2020).
Článok CAS PubMed Študovňa Google
- Mittal, V. Epiteliálny mezenchymálny prechod pri metastáze nádoru. Annu. Pathol. 13 , 395-412 (2018).
Článok CAS PubMed Študovňa Google
- Okabe, T. a kol. Mezenchymálne charakteristiky a prediktívne biomarkery na cirkulujúcich nádorových bunkách pre terapeutickú stratégiu. Cancers 12 , 3588-3610 (2020).
Článok CAS PubMed Central Študovňa Google
- Xu, J. a kol. Použitie technológie jednobunkového sekvenovania na detekciu cirkulujúcich nádorových buniek v solídnych nádoroch. Mol. Rakovina 20 , 104 (2021).
Článok PubMed PubMed Central Študovňa Google
- Wulfing, P. a kol. HER2-pozitívne cirkulujúce nádorové bunky naznačujú zlý klinický výsledok u pacientok s rakovinou prsníka v štádiu I až III. Clin. Cancer Res. 12 , 1715-1720 (2006).
- Hayashi, N. a kol. Prognostická hodnota HER2-pozitívnych cirkulujúcich nádorových buniek u pacientov s metastatickým karcinómom prsníka. Int J. Clin. Oncol. 17 , 96-104 (2012).
- Beije, N. a kol. Prognostický vplyv stavu HER2 a ER cirkulujúcich nádorových buniek u pacientov s metastatickým karcinómom prsníka s HER2-negatívnym primárnym nádorom. Neoplázia 18 , 647–653 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Wang, CH, Chang, CJ, Yeh, KY, Chang, PH & Huang, JS Prognostická hodnota HER2-pozitívnych cirkulujúcich nádorových buniek u pacientov s rakovinou prsníka: systematický prehľad a metaanalýza. Clin. Rakovina prsníka 17 , 341–349 (2017).
Článok CAS PubMed Študovňa Google
- Jaeger, BAS a kol. HER2 fenotyp cirkulujúcich nádorových buniek v HER2-pozitívnom včasnom karcinóme prsníka: projekt translačného výskumu prospektívnej randomizovanej štúdie fázy III. PLoS One 12 , e0173593 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Brouwer, A. a kol. Stav HER-2 cirkulujúcich nádorových buniek v skupine metastatického karcinómu prsníka: porovnávacia štúdia o technikách charakterizácie. PLoS One 14 , e0220906 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Chen, W. a kol. Detekcia HER2-pozitívnych cirkulujúcich nádorových buniek pomocou systému tekutej biopsie pri rakovine prsníka. Clin. Rakovina prsníka 19 , e239–e246 (2019).
Článok CAS PubMed Študovňa Google
- Jacot, W. a kol. Účinnosť HER2-amplifikovaných cirkulujúcich nádorových buniek pri HER2-negatívnom metastatickom karcinóme prsníka: štúdia CirCeT-DM1. Breast Cancer Res. 21 , 121 (2019).
Článok PubMed PubMed Central Študovňa Google
- Nanou, A., Zeune, LL, Bidard, FC, Pierga, JY & Terstappen, L. Expresia HER2 na extracelulárnych vezikulách odvodených od nádoru a cirkulujúcich nádorových bunkách pri metastatickej rakovine prsníka. Breast Cancer Res. 22 , 86 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Wang, C. a kol. Prognostická hodnota stavu HER2 na cirkulujúcich nádorových bunkách u pacientov s rakovinou prsníka v pokročilom štádiu s HER2-negatívnymi nádormi. Breast Cancer Res. Liečiť. 181 , 679-689 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Mishima, Y. a kol. Detekcia amplifikácie HER2 v cirkulujúcich nádorových bunkách HER2-negatívnych pacientov s rakovinou žalúdka. Cieľ Oncol. 12 , 341-351 (2017).
- Gradilone, A. a kol. Cirkulujúce nádorové bunky (CTC) pri metastatickej rakovine prsníka (MBC): prognóza, lieková rezistencia a fenotypová charakterizácia. Ann. Oncol. 22 , 86-92 (2011).
Článok CAS PubMed Študovňa Google
- Somlo, G. a kol. Viacnásobná expresia biomarkerov na cirkulujúcich nádorových bunkách v porovnaní s nádorovými tkanivami z primárnych a metastatických miest u pacientov s lokálne pokročilým / zápalovým karcinómom prsníka a štádiom IV s použitím novej technológie detekcie. Breast Cancer Res. Liečiť. 128 , 155-163 (2011).
Článok CAS PubMed PubMed Central Študovňa Google
- Forsare, C. a kol. Vývoj stavu estrogénového receptora od primárnych nádorov k metastázam a sériovo zhromaždeným cirkulujúcim nádorovým bunkám. Int. J. Mol. Sci. 21 , 2885-2897 (2020).
Článok CAS PubMed Central Študovňa Google
- Todenhofer, T. a kol. Predbežné skúsenosti s použitím systému adnatest (R) na detekciu cirkulujúcich nádorových buniek u pacientov s rakovinou prostaty. Anticancer Res. 32 , 3507-3513 (2012).
- Friedlander, TW a kol. Detekcia a charakterizácia invazívnych cirkulujúcich nádorových buniek odvodených od mužov s rakovinou prostaty rezistentnou na metastázu kastrácie. Int. J. Cancer 134 , 2284-2293 (2014).
Článok CAS PubMed Študovňa Google
- Yin, C. a kol. Molekulárne profilovanie spojených cirkulujúcich nádorových buniek od pacientov s rakovinou prostaty pomocou mikrofluidného zariadenia s duálnymi protilátkami. Anal. Chem. 90 , 3744-3751 (2018).
Článok CAS PubMed Študovňa Google
- Chen, L. a kol. Kombinované použitie EpCAM a FRalpha umožňuje vysoko účinné zachytenie cirkulujúcich nádorových buniek pri nemalobunkovom karcinóme pľúc. Sci. Rep. 8 , 1188 (2018).
Článok PubMed PubMed Central Študovňa Google
- Chen, X. a kol. Cirkulujúce nádorové bunky pozitívne na folátový receptor ako prediktívny biomarker pre účinnosť chemoterapie na báze pemetrexedu prvej línie u pacientov s neskvamóznym nemalobunkovým karcinómom pľúc. Ann. Prekl. Med. 8 , 631 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Wei, S. a kol. Účinok chirurgickej techniky na prvom mieste v žile vs. na prvom mieste na tepne na cirkulujúce nádorové bunky a prežitie u pacientov s nemalobunkovým karcinómom pľúc: randomizovaná klinická štúdia a analýza zhody skóre sklonu založená na registri. JAMA Surg. 154 , e190972 (2019).
Článok PubMed PubMed Central Študovňa Google
- Cao, W. a kol. Použitie detekcie cirkulujúcich nádorových buniek exprimujúcich survivín v periférnej krvi na predpovedanie recidívy nádoru po liečebnej resekcii rakoviny žalúdka. J. Surg. Oncol. 103 , 110-115 (2011).
- Krishnamurthy, S. a kol. Nesúlad v amplifikácii génu HER2 v cirkulujúcich a diseminovaných nádorových bunkách u pacientov s operabilným karcinómom prsníka. Cancer Med. 2 , 226-233 (2013).
Článok CAS PubMed PubMed Central Študovňa Google
- Bidard, FC a kol. Miera detekcie a prognostická hodnota cirkulujúcich nádorových buniek a cirkulujúcej nádorovej DNA pri metastatickom melanóme. Int. J. Cancer 134 , 1207-1213 (2014).
Článok CAS PubMed Študovňa Google
- Bettegowda, C. a kol. Detekcia cirkulujúcej nádorovej DNA v skorých a neskorých štádiách ľudských malignít. Sci. Prekl. Med. 6 , 224ra224 (2014).
- Lucci, A. a kol. Cirkulujúce nádorové bunky a skorá recidíva pri melanóme s pozitívnymi uzlinami. Clin. Cancer Res. 26 , 1886-1895 (2020).
Článok CAS PubMed Študovňa Google
- Hoshimoto, S. a kol. Hodnotenie prognostických cirkulujúcich nádorových buniek v štúdii fázy III adjuvantnej imunoterapie po kompletnej resekcii melanómu štádia IV. Ann. Surg. 255 , 357-362 (2012).
- Hoshimoto, S. a kol. Asociácia medzi cirkulujúcimi nádorovými bunkami a prognózou u pacientov s melanómom štádia III s metastázami sentinelových lymfatických uzlín v medzinárodnej multicentrickej štúdii fázy III. J. Clin. Oncol. 30 , 3819-3826 (2012).
Článok PubMed PubMed Central Študovňa Google
- Kiniwa, Y. a kol. Užitočnosť monitorovania cirkulujúcich nádorových buniek ako terapeutického biomarkera pri melanóme s mutáciou BRAF. BMC Cancer 21 , 287 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Hall, CS a kol. Cirkulujúce nádorové bunky u pacientov s melanómom v štádiu IV. J. Am. Zb. Surg. 227 , 116 – 124 (2018).
- Lin, SY a kol. Prospektívne molekulárne profilovanie cirkulujúcich nádorových buniek od pacientov s melanómom, ktorí dostávajú kombinatorickú imunoterapiu. Clin. Chem. 66 , 169-177 (2020).
Článok PubMed PubMed Central Študovňa Google
- Maheswaran, S. a kol. Detekcia mutácií v EGFR v cirkulujúcich bunkách rakoviny pľúc. N. Engl. J. Med. 359 , 366-377 (2008).
Článok CAS PubMed PubMed Central Študovňa Google
- Fabbri, F. a kol. Detekcia a obnova cirkulujúcich buniek rakoviny hrubého čreva pomocou zariadenia na báze dielektroforézy: Stav mutácie KRAS v čistých CTC. Cancer Lett. 335 , 225 – 231 (2013).
Článok CAS PubMed Študovňa Google
- Buim, ME a kol. Detekcia mutácií KRAS v cirkulujúcich nádorových bunkách od pacientov s metastatickým kolorektálnym karcinómom. Cancer Biol. Ther. 16 , 1289-1295 (2015).
Článok CAS PubMed PubMed Central Študovňa Google
- Kalikaki, A. a kol. Genotypové zmeny KRAS cirkulujúcich nádorových buniek počas liečby pacientov s metastatickým kolorektálnym karcinómom. PloS One 9 , e104902 (2014).
Článok PubMed PubMed Central Študovňa Google
- Kondo, Y. a kol. Analýza mutácie KRAS jednotlivých cirkulujúcich nádorových buniek od pacientov s metastatickým kolorektálnym karcinómom. BMC Cancer 17 , 311 (2017).
Článok PubMed PubMed Central Študovňa Google
- Kulemann, B. a kol. Rakovina pankreasu: cirkulujúce nádorové bunky a primárne nádory vykazujú heterogénne mutácie KRAS. Sci. Rep. 7 , 4510 (2017).
Článok PubMed PubMed Central Študovňa Google
- Lohr, JG a kol. Celoexómové sekvenovanie cirkulujúcich nádorových buniek poskytuje okno do metastatického karcinómu prostaty. Nat. Biotechnol. 32 , 479-484 (2014).
Článok CAS PubMed PubMed Central Študovňa Google
- Faugeroux, V. a kol. Prístupný a jedinečný pohľad na mutačný obsah metastáz prostredníctvom celoexómového sekvenovania cirkulujúcich nádorových buniek pri metastatickej rakovine prostaty. Eur. Urol. Oncol. 3 , 498-508 (2020).
- Deng, G. a kol. Jednobunková mutačná analýza PIK3CA v cirkulujúcich nádorových bunkách a metastázach pri rakovine prsníka odhaľuje heterogenitu, nesúlad a pretrvávanie mutácií v kultivovaných diseminovaných nádorových bunkách z kostnej drene. BMC Cancer 14 , 456-467 (2014).
Článok PubMed PubMed Central Študovňa Google
- Fernandez, V. a kol. Mutácie TP53 zistené v cirkulujúcich nádorových bunkách prítomných v krvi metastatických pacientok s trojnásobne negatívnym karcinómom prsníka. Breast Cancer Res. 16 , 445 (2014).
Článok PubMed PubMed Central Študovňa Google
- Kelley, RK a kol. Cirkulujúce nádorové bunky pri hepatocelulárnom karcinóme: pilotná štúdia detekcie, počítania a sekvenovania ďalšej generácie v prípadoch a kontrolách. BMC Cancer 15 , 206 (2015).
Článok PubMed PubMed Central Študovňa Google
- Ni, X. a kol. Reprodukovateľné vzory variácií počtu kópií medzi jednotlivými cirkulujúcimi nádorovými bunkami pacientov s rakovinou pľúc. Proc. Natl Acad. Sci. USA 110 , 21083 – 21088 (2013).
Článok CAS PubMed PubMed Central Študovňa Google
- Carter, L. a kol. Molekulárna analýza cirkulujúcich nádorových buniek identifikuje odlišné profily počtu kópií u pacientov s chemosenzitívnym a chemorefraktérnym malobunkovým karcinómom pľúc. Nat. Med. 23 , 114-119 (2017).
Článok CAS PubMed Študovňa Google
- Paoletti, C. a kol. Komplexné profilovanie mutácií a počtu kópií v archivovaných cirkulujúcich nádorových bunkách rakoviny prsníka dokumentuje mechanizmy heterogénnej rezistencie. Cancer Res. 78 , 1110-1122 (2018).
Článok CAS PubMed Študovňa Google
- Ortolan, E. a kol. Krvná genomika trojnásobne negatívnej progresie rakoviny prsníka u pacientov liečených neoadjuvantchemoterapiou. ESMO Open 6 , 100086 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Lambros, MB a kol. Jednobunkové analýzy tekutých biopsií rakoviny prostaty získaných aferézou. Clin. Cancer Res.: . J. Am. Doc. Cancer Res. 24 , 5635-5644 (2018).
- Gupta, S. a kol. Zmeny počtu kópií celého genómu v cirkulujúcich nádorových bunkách od mužov s metastatickou kastráciou rezistentnou rakovinou prostaty rezistentnou na abiraterón orenzalutamid. Clin. Cancer Res.: . J. Am. Doc. Cancer Res. 23 , 1346-1357 (2017).
- Malihi, PD a kol. Analýza jednobunkových cirkulujúcich nádorových buniek odhaľuje genómovú nestabilitu ako charakteristický znak agresívnej rakoviny prostaty. Clin. Cancer Res.: . J. Am. Doc. Cancer Res. 26 , 4143-4153 (2020).
- Pailler, E. a kol. Detekcia cirkulujúcich nádorových buniek, ktoré nesú jedinečné preskupenie ALK pri ALK-pozitívnej nemalobunkovej rakovine. J. Clin. Oncol. 31 , 2273-2281 (2013).
- Mayer, JA a kol. Stanovenie stavu HER2 na základe FISH v cirkulujúcich nádorových bunkách izolovaných s mikrofluidnou platformou CEE. Cancer Genet. 204 , 589-595 (2011).
Článok CAS PubMed Študovňa Google
- Frithiof, H., Aaltonen, K. & Ryden, L. Metóda založená na FISH na hodnotenie stavu amplifikácie HER-2 v cirkulujúcich nádorových bunkách rakoviny prsníka po izolácii CellSearch. OncoTargets Ther. 9 , 7095-7103 (2016).
- Gkountela, S. a kol. Cirkulujúce zhlukovanie nádorových buniek formuje metyláciu DNA, aby umožnilo naočkovanie metastáz. Cell 176 , 98-112.e114 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Dong, Y., Wang, Z. & Shi, Q. Profilovanie jednobunkového transkriptómu založené na tekutej biopsii charakterizuje heterogenitu diseminovaných nádorových buniek z pľúcneho adenokarcinómu. Proteomics 20 , e1900224 (2020).
- Magbanua, MJM a kol. Rozšírené genómové profilovanie cirkulujúcich nádorových buniek u pacientov s metastatickým karcinómom prsníka na posúdenie stavu biomarkerov a biológie v priebehu času (CALGB 40502 a CALGB 40503, Alliance). Clin. Cancer Res.: . J. Am. Doc. Cancer Res. 24 , 1486-1499 (2018).
- Cheng, Y.-H. a kol. Hydro-Seq umožňuje vysokovýkonné jednobunkové sekvenovanie RNA bez kontaminácie pre cirkulujúce nádorové bunky. Nat. komun. 10 , 2163-2173 (2019).
Článok PubMed PubMed Central Študovňa Google
- Miyamoto, D. a kol. RNA-Seq jednotlivých CTC prostaty implikuje nekanonickú Wnt signalizáciu v antiandrogénovej rezistencii. Science 349 , 1351 – 1356 (2015).
Článok CAS PubMed PubMed Central Študovňa Google
- Barbazan, J. a kol. Molekulárna charakterizácia cirkulujúcich nádorových buniek u ľudského metastatického kolorektálneho karcinómu. PloS One 7 , e40476 (2012).
Článok CAS PubMed PubMed Central Študovňa Google
- Kallergi, G. a kol. Markery epitelového až mezenchymálneho prechodu exprimované v cirkulujúcich nádorových bunkách u pacientov so skorým a metastatickým karcinómom prsníka. Breast Cancer Res. 13 , R59 (2011).
Článok PubMed PubMed Central Študovňa Google
- Balasubramanian, P. a kol. Multiparametrová analýza, vrátane EMT markerov, na negatívne obohatených vzorkách krvi od pacientov so skvamocelulárnym karcinómom hlavy a krku. PLoS One 7 , e42048 (2012).
Článok CAS PubMed PubMed Central Študovňa Google
- Theodoropoulos, PA a kol. Cirkulujúce nádorové bunky s predpokladaným fenotypom kmeňových buniek v periférnej krvi pacientov s rakovinou prsníka. Cancer Lett. 288 , 99-106 (2010).
Článok CAS PubMed Študovňa Google
- Armstrong, AJ a kol. Cirkulujúce nádorové bunky od pacientov s pokročilým karcinómom prostaty a prsníka vykazujú oba epitelové aj mezenchymálne markery. Mol. Cancer Res. 9 , 997-1007 (2011).
Článok CAS PubMed PubMed Central Študovňa Google
- Liu, X. a kol. Bunky systémového karcinómu prsníka epitelového typu s obmedzeným mezenchymálnym prechodom sú hlavným zdrojom metastáz. Sci. Adv. 5 , eaav4275 (2019).
Článok PubMed PubMed Central Študovňa Google
- Thiery, JP & Lim, CT Diseminácia nádoru: záležitosť EMT. Cancer Cell 23 , 272-273 (2013).
Článok CAS PubMed Študovňa Google
- Pečot, CV a kol. Nová platforma na detekciu CK+ a CK- CTC. Cancer Discov. 1 , 580-586 (2011).
Článok CAS PubMed PubMed Central Študovňa Google
- Sun, YF a kol. Cirkulujúce nádorové bunky z rôznych vaskulárnych miest vykazujú priestorovú heterogenitu v epiteliálnom a mezenchymálnom zložení a zreteľný klinický význam pri hepatocelulárnom karcinóme. Clin. Cancer Res.: . J. Am. Doc. Cancer Res. 24 , 547-559 (2018).
- Xu, L. a kol. Nová asociácia cirkulujúcich nádorových buniek a cirkulujúcich megakaryocytov s prognózou rakoviny prostaty. Clin. Cancer Res. 23 , 5112-5122 (2017).
Článok CAS PubMed Študovňa Google
- Dongre, A. & Weinberg, RA Nové poznatky o mechanizmoch epitelovo-mezenchymálneho prechodu a dôsledkoch rakoviny. Nat. Mol. Cell Bio 20 , 69-84 (2019).
- Guan, Y. a kol. Identifikácia kľúčových génov a funkcií cirkulujúcich nádorových buniek u viacerých druhov rakoviny prostredníctvom bioinformatickej analýzy. BMC Med. Genom. 13 , 140 (2020).
- Tashireva, LA a kol. Heterogénne prejavy epiteliálno-mezenchymálnej plasticity cirkulujúcich nádorových buniek u pacientov s rakovinou prsníka. Int. J. Mol. Sci. 22 , 2504-2521 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Xin, Y., Li, K., Yang, M. & Tan, Y. Fluidný šmykový stres indukuje EMT cirkulujúcich nádorových buniek prostredníctvom jnk signalizácie v prospech ich prežitia počas hematogénneho šírenia. Int. J. Mol. Sci. 21 , 8115-8130 (2020).
Článok CAS PubMed Central Študovňa Google
- Horimoto, Y. a kol. Analýza stavu cirkulujúcich nádorových buniek a stavu epitelového mezenchymálneho prechodu (EMT) počas liečby založenej na eribulíne u 22 pacientov s metastatickým karcinómom prsníka: pilotná štúdia. J. Transl. Med. 16 , 287 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Guan, XW a kol. Prognostické a terapeutické dôsledky detekcie fenotypu cirkulujúcich nádorových buniek na základe markerov epiteliálno-mezenchymálnych prechodov v chemoterapii prvej línie HER2-negatívneho metastatického karcinómu prsníka. CancerCommun 39 , 1–10 (2019).
- Lindsay, CR a kol. Prospektívne vyšetrenie profilov cirkulujúcich nádorových buniek v molekulárnych podskupinách nemalobunkového karcinómu pľúc. Ann. Oncol. 28 , 1523 – 1531 (2017).
Článok CAS PubMed Študovňa Google
- Satelli, A. a kol. Zachytenie epitelovo-mezenchymálnych prechodných cirkulujúcich nádorových buniek na detekciu progresie nádoru. Clin. Cancer Res. 21 , 899-906 (2015).
Článok CAS PubMed Študovňa Google
- Brechbuhl, HM a kol. Analýza heterogenity buniek rakoviny prsníka v obehu a interakcií s mononukleárnymi bunkami periférnej krvi. Mol. Carcinog. 59 , 1129-1139 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Miklíková, S. a kol. Skóre založené na zápale zvyšuje prognostickú hodnotu cirkulujúcich nádorových buniek pri primárnej rakovine prsníka. Cancers 12 , 1134–1148 (2020).
Článok CAS PubMed Central Študovňa Google
- Wu, Y. a kol. SUMOylácia potláča expresiu Nanog prostredníctvom modulujúcich transkripčných faktorov Oct4 a Sox2. PloS One 7 , e39606 (2012).
Článok CAS PubMed PubMed Central Študovňa Google
- Zhang, R. a kol. Koexpresia kmeňových buniek a epiteliálnych mezenchymálnych prechodových markerov v cirkulujúcich nádorových bunkách pacientov s rakovinou močového mechúra. OncoTargets Ther. 13 , 10739-10748 (2020).
- Zhao, P. a kol. Založenie a charakterizácia CTC bunkovej línie z periférnej krvi pacienta s rakovinou prsníka. J. Cancer 10 , 6095-6104 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Wan, S. a kol. Nové labyrintové mikrofluidné zariadenie deteguje cirkulujúce nádorové bunky exprimujúce marker rakovinových kmeňových buniek a cirkulujúce nádorové mikroembólie v hepatocelulárnom karcinóme. Sci. Rep. 9 , 18575 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Liu, T. a kol. Cirkulujúce gliómové bunky vykazujú vlastnosti podobné kmeňovým bunkám. Cancer Res. 78 , 6632-6642 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Yin, J. a kol. Cirkulujúce nádorové bunky obohatené depléciou leukocytov s bi-protilátkami pri nemalobunkovom karcinóme pľúc: potenciálna klinická aplikácia. PloS One 10 , e0137076 (2015).
Článok PubMed PubMed Central Študovňa Google
- Jin, J., Tang, K., Xin, Y., Zhang, T. & Tan, Y. Hemodynamický šmykový tok reguluje biofyzikálne charakteristiky a funkcie cirkulujúcich buniek nádoru prsníka pripomínajúcich mozgové metastázy. Soft Matter 14 , 9528-9533 (2018).
Článok CAS PubMed Študovňa Google
- Choi, H. a kol. Hydrodynamické šmykové napätie podporuje epitelovo-mezenchymálny prechod znížením aktivity ERK a GSK3p. Breast Cancer Res. 21 , 6 (2019).
Článok PubMed PubMed Central Študovňa Google
- Follain, G. a kol. Kvapaliny a ich mechanika pri tranzite nádoru: formovanie metastáz. Nat. Rev. Cancer 20 , 107-124 (2020).
Článok CAS PubMed Študovňa Google
- Strilic, B. & Offermanns, S. Intravaskulárne prežitie a extravazácia nádorových buniek. Cancer cell 32 , 282-293 (2017).
Článok CAS PubMed Študovňa Google
- Rejniak, KA Cirkulujúce nádorové bunky: keď sa solídny nádor stretne s tekutým mikroprostredím. Adv. Exp. Med. Biol. 936 , 93-106 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Garrido-Navas, C. a kol. Kooperatívne a únikové mechanizmy medzi cirkulujúcimi nádorovými bunkami a krvnými zložkami. Cells 8 , 1382-1391 (2019).
Článok CAS PubMed Central Študovňa Google
- Shaul, ME & Fridlender, ZG Neutrofily spojené s nádorom u pacientov s rakovinou. Nat. Clin. Oncol. 16 , 601-620 (2019).
- Aliustaoglu, M. a kol. Vplyv hodnôt periférnej krvi na prognózu pacientov s lokálne pokročilým karcinómom žalúdka pred liečbou. Med. Oncol. 27 , 1060-1065 (2010).
- Hu, S. a kol. Predoperačný počet monocytov v periférnej krvi je spojený s pečeňovými metastázami a celkovým prežívaním pacientov s inkolorektálnym karcinómom. PloS One 11 , e0157486 (2016).
Článok PubMed PubMed Central Študovňa Google
- Wang, Y. a kol. Cirkulujúce neutrofily predpovedajú slabé prežitie HCC a podporujú progresiu HCC prostredníctvom signálnej dráhy p53 a STAT3. J. Cancer 11 , 3736-3744 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Stott, SL a kol. Izolácia cirkulujúcich nádorových buniek pomocou čipu rybej kosti generujúceho mikrovortex. Proc. Natl Acad. Sci. USA 107 , 18392 – 18397 (2010).
Článok CAS PubMed PubMed Central Študovňa Google
- Szczerba, BM a kol. Neutrofily sprevádzajú cirkulujúce nádorové bunky, aby umožnili progresiu bunkového cyklu. Nature 566 , 553–557 (2019).
Článok CAS PubMed Študovňa Google
- Hattar, K. a kol. Interakcie medzi neutrofilmi a bunkami nemalobunkového karcinómu pľúc: zvýšenie proliferácie nádoru a syntéza zápalových mediátorov. Cancer Immunol., Immunother. 63 , 1297-1306 (2014).
- Spicer, JD a kol. Neutrofily podporujú metastázy v pečeni prostredníctvom interakcií sprostredkovaných Mac-1 s cirkulujúcimi nádorovými bunkami. Cancer Res. 72 , 3919-3927 (2012).
Článok CAS PubMed Študovňa Google
- Strell, C., Lang, K., Niggemann, B., Zaenker, KS & Entschladen, F. Povrchové molekuly regulujúce rolovanie a adhéziu k endotelu neutrofilných granulocytov a buniek karcinómu prsníka MDA-MB-468 a ich interakcia. Cell. Mol. život Sci. 64 , 3306-3316 (2007).
Článok CAS PubMed Študovňa Google
- Huh, SJ, Liang, S., Sharma, A., Dong, C. & Robertson, GP Prechodne zachytené cirkulujúce nádorové bunky interagujú s neutrofilmi, aby sa uľahčil rozvoj pľúcnych metastáz. Cancer Res. 70 , 6071-6082 (2010).
Článok CAS PubMed PubMed Central Študovňa Google
- Rowson-Hodel, AR a kol. Membránový mucín Muc4 podporuje spojenie krvných buniek s nádorovými bunkami a sprostredkováva účinné metastázy v myšom modeli rakoviny prsníka. Oncogene 37 , 197-207 (2018).
Článok CAS PubMed Študovňa Google
- Chen, MB a kol. Zapálené neutrofily sekvestrované na zachytených nádorových bunkách prostredníctvom chemotaktického obmedzenia podporujú extravazáciu nádorových buniek. Proc. Natl Acad. Sci. USA 115 , 7022 – 7027 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Masucci, MT, Minopoli, M., Del Vecchio, S. & Carriero, MV Vznikajúca úloha neutrofilných extracelulárnych pascí (NET) v progresii nádoru a metastázach. Predné. Immunol. 11 , 1749 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Cools-Lartigue, J. a kol. Neutrofilné extracelulárne pasce sekvestrujú cirkulujúce nádorové bunky a podporujú metastázy. J. Clin. Vyšetrovať. 123 , 3446-3458 (2013).
Článok CAS PubMed Central Študovňa Google
- Najmeh, S. a kol. Neutrofilné extracelulárne pasce sekvestrujú cirkulujúce nádorové bunky prostredníctvom interakcií sprostredkovaných a1-integrínom. Int. J. Cancer 140 , 2321-2330 (2017).
Článok CAS PubMed Študovňa Google
- Tohme, S. a kol. Neutrofilné extracelulárne pasce podporujú rozvoj a progresiu pečeňových metastáz po chirurgickom strese. Cancer Res. 76 , 1367-1380 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Albrengues, J. a kol. Neutrofilné extracelulárne pasce vytvorené počas zápalu prebúdzajú u myší spiace rakovinové bunky. Science 361 , 1353–1367 (2018).
- Xiao, Y. a kol. Katepsín C podporuje pľúcne metastázy rakoviny prsníka moduláciou infiltrácie neutrofilov a tvorby extracelulárnej pasce neutrofilov. Cancer Cell 39 , 423-437.e427 (2021).
Článok CAS PubMed Študovňa Google
- Yang, L. a kol. DNA neutrofilných extracelulárnych pascí podporuje metastázy rakoviny prostredníctvom CCDC25. Nature 583 , 133-138 (2020).
Článok CAS PubMed Študovňa Google
- Zhang, J. a kol. Cirkulujúce neutrofily spojené s nádorom (cTAN) prispievajú k prežitiu cirkulujúcich nádorových buniek potlačením aktivácie periférnych leukocytov. Tumor Biol.: J. Int. Soc. Oncodev. Biol. Med. 37 , 5397-5404 (2016).
- Spiegel, A. a kol. Neutrofily potláčajú klírens nádorových buniek sprostredkovaný intraluminálnymi nk bunkami a zvyšujú extravazáciu diseminovaných buniek karcinómu. Cancer Discov. 6 , 630-649 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Kumagai, Y. a kol. Chirurgický stres zvyšuje cirkulujúce neutrofily s nízkou hustotou, čo môže podporovať recidívu nádoru. J. Surg. Res. 246 , 52 – 61 (2020).
Článok CAS PubMed Študovňa Google
- Coffelt, SB a kol. Produkujúci IL-17 ?? T bunky a neutrofily podporujú metastázy rakoviny prsníka. Nature 522 , 345–348 (2015).
Článok CAS PubMed PubMed Central Študovňa Google
- Doak, GR, Schwertfeger, KL & Wood, DK Vzdialené vzťahy: funkcie makrofágov v metastatickej nike. TrendsCancer 4 , 445–459 (2018).
- Hamilton, G., Rath, B., Klameth, L. & Hochmair, MJ Malobunkový karcinóm pľúc: nábor makrofágov cirkulujúcimi nádorovými bunkami. Oncoimmunology 5 , e1093277 (2016).
- Hamilton, G. & Rath, B. Interakcie cirkulujúcich nádorových buniek s makrofágmi: dôsledky pre biológiu a liečbu. Prekl. Lung Cancer Res. 6 , 418-430 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Wei, C. a kol. Pre metastázy kolorektálneho karcinómu sprostredkované mezenchymálnymi cirkulujúcimi nádorovými bunkami sú potrebné presluchy medzi rakovinovými bunkami a makrofágmi spojenými s nádorom. Mol. Rakovina 18 , 64 (2019).
Článok PubMed PubMed Central Študovňa Google
- Osmulski, PA a kol. Kontakty s makrofágmi podporujú agresívny nanomechanický fenotyp cirkulujúcich nádorových buniek pri rakovine prostaty. Cancer Res. 81 , 4110-4123 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Shabo, I. a kol. Makrofágové znaky v rakovinových bunkách sú indukované fúziou makrofágov a rakovinových buniek a nemožno ich vysvetliť bunkovou interakciou. BMC Cancer 15 , 922 (2015).
Článok PubMed PubMed Central Študovňa Google
- Clawson, GA a kol. Fúzie makrofágov a nádorových buniek z periférnej krvi pacientov s melanómom. PloS One 10 , e0134320 (2015).
Článok PubMed PubMed Central Študovňa Google
- Clawson, GA a kol. „Stealth diseminácia“ fúzií makrofág-nádorových buniek kultivovaných z krvi pacientov s duktálnym adenokarcinómom pankreasu. PloS One 12 , e0184451 (2017).
Článok PubMed PubMed Central Študovňa Google
- Manjunath, Y. a kol. Fúzne bunky nádor-bunka-makrofág ako tekuté biomarkery a zosilňovače nádorov pri rakovine. Int. J. Mol. Sci. 21 , 1872 (2020).
Článok CAS PubMed Central Študovňa Google
- Gast, CE a kol. Bunková fúzia potencuje heterogenitu nádoru a odhaľuje cirkulujúce hybridné bunky, ktoré korelujú so štádiom a prežitím. Sci. Adv. 4 , eaat7828 (2018).
Článok PubMed PubMed Central Študovňa Google
- Manjunath, Y. a kol. Cirkulujúce obrovské nádorovo-makrofágové fúzne bunky sú nezávislými prognostikami u pacientov s NSCLC. J. Thorac. Oncol.: . Publ. Int. Doc. Štúdia rakoviny pľúc 15 , 1460–1471 (2020).
- Schlesinger, M. Úloha krvných doštičiek a receptorov krvných doštičiek v metastázach rakoviny. J. Hematol. Oncol. 11 , 125 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Gaertner, F. & Massberg, S. Hliadka na cievnych hraniciach: krvné doštičky v imunite voči infekcii a rakovine. Nat. Rev. Immunol. 19 , 747-760 (2019).
Článok CAS PubMed Študovňa Google
- Thomas, GM a kol. Tkanivový faktor vyjadrený cirkulujúcimi mikročasticami získanými z rakovinových buniek drasticky zvyšuje výskyt hlbokej žilovej trombózy u myší. J. trombóza Haemost. 13 , 1310-1319 (2015).
- Stark, K. a kol. Odlišná patogenéza venóznej trombózy spojenej s mikrovezikulami rakoviny pankreasu identifikuje nové antitrombotické ciele in vivo. Arterioskleróza, trombóza, Vasc. Biol. 38 , 772-786 (2018).
- Labelle, M., Begum, S. & Hynes, RO Priama signalizácia medzi krvnými doštičkami a rakovinovými bunkami indukuje epiteliálny mezenchymálny prechod a podporuje metastázy. Cancer Cell 20 , 576-590 (2011).
Článok CAS PubMed PubMed Central Študovňa Google
- Guo, Y., Cui, W., Pei, Y. & Xu, D. Krvné doštičky podporujú inváziu a indukujú prechod z epitelu na mezenchymálny v bunkách rakoviny vaječníkov prostredníctvom TGF-? signálna dráha. Gynecol. Oncol. 153 , 639-650 (2019).
Článok CAS PubMed Študovňa Google
- Xiong, G. a kol. Hsp47 podporuje metastázy rakoviny zvýšením interakcie rakovinových buniek a krvných doštičiek závislej od kolagénu. Proc. Natl Acad. Sci. USA 117 , 3748-3758 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Egan, K., Cooke, N. & Kenny, D. Život v šmyku: krvné doštičky chránia rakovinové bunky pred poškodením spôsobeným šmykom. Clin. Exp. Metastasis 31 , 697-704 (2014).
- Haemmerle, M. a kol. Krvné doštičky znižujú anoikis a podporujú metastázy aktiváciou signalizácie YAP1. Nat. komun. 8 , 310 (2017).
Článok PubMed PubMed Central Študovňa Google
- Nieswandt, B., Hafner, M., Echtenacher, B. & Männel, DN Lýze nádorových buniek prirodzenými zabíjačskými bunkami u myší bránia krvné doštičky. Cancer Res. 59 , 1295-1300 (1999).
- Placke, T. a kol. MHC triedy I odvodený z krvných doštičiek prepožičiava rakovinovým bunkám pseudonormálny fenotyp, ktorý podvracia protinádorovú reaktivitu prirodzených zabíjačských imunitných buniek. Cancer Res. 72 , 440-448 (2012).
Článok CAS PubMed Študovňa Google
- Kopp, HG, Placke, T. & Salih, HR Transformačný rastový faktor-beta odvodený z krvných doštičiek down-reguluje NKG2D, čím inhibuje protinádorovú reaktivitu prirodzených zabíjačských buniek. Cancer Res. 69 , 7775-7783 (2009).
Článok CAS PubMed Študovňa Google
- Maurer, S. a kol. Doštičkami sprostredkované vylučovanie NKG2D ligandov zhoršuje NK bunkový imunitný dohľad nad nádorovými bunkami. Oncoimmunology 7 , e1364827 (2018).
- Placke, T., Salih, HR & Kopp, HG GITR ligand poskytovaný trombopoetickými bunkami inhibuje protinádorovú aktivitu NK buniek. J. Immunol. 189 , 154-160 (2012).
Článok CAS PubMed Študovňa Google
- Ren, J. a kol. Os trombocytov TLR4-ERK5 uľahčuje sieťovo sprostredkované zachytenie cirkulujúcich nádorových buniek a vzdialených metastáz po chirurgickom strese. Cancer Res. 81 , 2373-2385 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Rachidi, S. a kol. Krvné doštičky podvracajú T bunkovú imunitu proti rakovine prostredníctvom osi GARP-TGFp. Sci. Immunol. 2 , 7911-7937 (2017).
- Xiang, B. a kol. Krvné doštičky chránia pred septickým šokom inhibíciou zápalu závislého od makrofágov prostredníctvom signálnej dráhy cyklooxygenázy 1. Nat. komun. 4 , 2657 (2013).
- Bendas, G. & Borsig, L. Adhézia a metastáza rakovinových buniek: selektíny, integríny a inhibičný potenciál heparínov. Int. J. Cell Biol. 2012 , 676731 (2012).
- Lonsdorf, AS a kol. Zapojenie αIIbβ3 (GPIIb/IIIa) s integrínom ανβ3 sprostredkuje interakciu buniek melanómu s krvnými doštičkami: spojenie s hematogénnymi metastázami. J. Biol. Chem. 287 , 2168-2178 (2012).
Článok CAS PubMed Študovňa Google
- Coupland, LA, Chong, BH & Parish, CR doštičky a P-selektín kontrolujú metastázy nádorových buniek orgánovo špecifickým spôsobom a nezávisle od NK buniek. Cancer Res. 72 , 4662-4671 (2012).
Článok CAS PubMed Študovňa Google
- Schumacher, D., Strilic, B., Sivaraj, KK, Wettschureck, N. & Offermanns, S. Nukleotidy odvodené z krvných doštičiek podporujú migráciu transendotelu nádorových buniek a metastázy prostredníctvom receptora P2Y2. Cancer Cell 24 , 130-137 (2013).
Článok CAS PubMed Študovňa Google
- Mammadova-Bach, E. a kol. Integrín krvných doštičiek a6p1 kontroluje pľúcne metastázy prostredníctvom priamej väzby na ADAM9 pochádzajúci z rakovinových buniek. JCI Insight 1 , e88245 (2016).
Článok PubMed PubMed Central Študovňa Google
- Ward, Y. a kol. Krvné doštičky podporujú metastázy väzbou nádorového CD97, čo vedie k obojsmernej signalizácii, ktorá koordinuje transendotelovú migráciu. Cell Rep. 23 , 808-822 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Mammadova-Bach, E. a kol. Doštičkový glykoproteín VI podporuje metastázy prostredníctvom interakcie s galektínom-3 odvodeným z rakovinových buniek. Blood 135 , 1146-1160 (2020).
- Xu, Y. a kol. Blokáda krvných doštičiek pomocou nádorovo špecifických nanočastíc uvoľňujúcich NO zabraňuje metastázovaniu nádoru a reverznej imunosupresii nádoru. ACS Nano 14 , 9780-9795 (2020).
Článok CAS PubMed Študovňa Google
- Cassetta, L. a kol. Diferenciálna expanzia cirkulujúcich ľudských podskupín MDSC u pacientov s rakovinou, infekciou a zápalom. J. Immunother. Cancer 8 , 1223-1235 (2020).
- Liu, Q., Liao, Q. & Zhao, Y. Myeloidné supresorové bunky (MDSC) uľahčujú vzdialené metastázy malignít tým, že chránia cirkulujúce nádorové bunky (CTC) pred imunitným dohľadom. Med. Hypotézy 87 , 34–39 (2016).
Článok CAS PubMed Študovňa Google
- Jiménez-Cortegana, C. a kol. Cirkulujúce supresorové bunky odvodené od myeloidov a regulačné T bunky ako imunologické biomarkery pri refraktérnom/recidivujúcom difúznom veľkom B-bunkovom lymfóme: translačné výsledky zo štúdie R2-GDP-GOTEL. J. Immunother. Cancer 9 , 2323-2334 (2021).
- Sprouse, ML a kol. PMN-MDSC zlepšujú metastatické vlastnosti CTC prostredníctvom recipročných interakcií prostredníctvom ROS/Notch/nodálnej signalizácie. Int. J. Mol. Sci. 20 , 1916–1935 (2019).
Článok CAS PubMed Central Študovňa Google
- Chen, X. & Song, E. Premena nepriateľov na priateľov: zameranie sa na fibroblasty súvisiace s rakovinou. Nat. Drug Discov. 18 , 99-115 (2019).
Článok CAS PubMed Študovňa Google
- Gaggioli, C. a kol. Fibroblastmi vedená kolektívna invázia buniek karcinómu s rôznymi úlohami pre RhoGTPázy vo vedúcich a nasledujúcich bunkách. Nat. Cell Biol. 9 , 1392-1400 (2007).
Článok CAS PubMed Študovňa Google
- Duda, DG a kol. Malígne bunky uľahčujú pľúcne metastázy tým, že si prinesú vlastnú pôdu. Proc. Natl Acad. Sci. USA 107 , 21677-21682 (2010).
Článok CAS PubMed PubMed Central Študovňa Google
- Ortiz-Otero, N. a kol. Fibroblasty spojené s rakovinou prepožičiavajú cirkulujúcim nádorovým bunkám odolnosť proti šmyku počas metastatickej progresie rakoviny prostaty. Oncotarget 11 , 1037–1050 (2020).
Článok PubMed PubMed Central Študovňa Google
- Ao, Z. a kol. Identifikácia fibroblastov spojených s rakovinou v cirkulujúcej krvi od pacientov s metastatickým karcinómom prsníka. Cancer Res. 75 , 4681-4687 (2015).
Článok CAS PubMed Študovňa Google
- Jiang, R. a kol. Rýchla izolácia cirkulujúcich fibroblastov spojených s rakovinou akustickým mikrostreamingom na hodnotenie metastatickej náchylnosti pacientov s rakovinou prsníka. Lab. Čip 969-981 (2020).
- Shen, Z., Wu, A. & Chen, X. Súčasné detekčné technológie pre cirkulujúce nádorové bunky. Chem. Soc. Rev. 46 , 2038-2056 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Vona, G. a kol. Izolácia epitelových nádorových buniek podľa veľkosti – nová metóda na imunomorfologickú a molekulárnu charakterizáciu cirkulujúcich nádorových buniek. Am. J. Pathol. 156 , 57-63 (2000).
Článok CAS PubMed PubMed Central Študovňa Google
- Harouaka, RA a kol. Flexibilné mikropružinové zariadenie na vysokovýkonné obohatenie životaschopných cirkulujúcich nádorových buniek. Clin. Chem. 60 , 323-333 (2014).
Článok CAS PubMed Študovňa Google
- Rosenberg, R. a kol. Porovnanie dvoch centrifugačných systémov s hustotným gradientom na obohatenie diseminovaných nádorových buniek v krvi. Cytometry 49 , 150-158 (2002).
Článok CAS PubMed Študovňa Google
- Gupta, V. a kol. ApoStream(), nové dielektroforetické zariadenie na izoláciu nezávislú od protilátok a obnovu životaschopných rakovinových buniek z krvi. Biomicrofluidics 6 , 24133 (2012).
- Sajay, BN a kol. Mikrofluidná platforma na negatívne obohatenie cirkulujúcich nádorových buniek. Biomed. Microdevices 16 , 537-548 (2014).
Článok CAS PubMed Študovňa Google
- Allard, WJ a kol. Nádorové bunky cirkulujú v periférnej krvi všetkých závažných karcinómov, ale nie u zdravých jedincov alebo pacientov s nezhubnými ochoreniami. Clin. Cancer Res. 10 , 6897-6904 (2004).
- Talasaz, AH a kol. Izolácia vysoko obohatených populácií cirkulujúcich epiteliálnych buniek a iných vzácnych buniek z krvi pomocou magnetického zametacie zariadenia. Proc. Natl Acad. Sci. USA 106 , 3970-3975 (2009).
Článok CAS PubMed PubMed Central Študovňa Google
- Wu, S. a kol. Obohatenie a počítanie cirkulujúcich nádorových buniek účinnou depléciou leukocytových frakcií. Clin. Chem. Lab. Med. 53 , 337 (2015).
Článok CAS PubMed Študovňa Google
- Nasiri, R. a kol. Mikrofluidné prístupy v cielenej separácii buniek/častíc na základe fyzikálnych vlastností: základy a aplikácie. Malý 16 , e2000171 (2020).
- Nagrath, S. a kol. Izolácia vzácnych cirkulujúcich nádorových buniek u pacientov s rakovinou technológiou mikročipov. Nature 450 , 1235-1239 (2007).
Článok CAS PubMed PubMed Central Študovňa Google
- Park, MH a kol. Zlepšená izolácia a uvoľňovanie cirkulujúcich nádorových buniek pomocou väzby nanočastíc a výmeny ligandov v mikrofluidnom čipe. J. Am. Chem. Soc. 139 , 2741 – 2749 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Fachin, F. a kol. Monolitický čip na vysokovýkonné odbúravanie krviniek na triedenie vzácnych cirkulujúcich nádorových buniek. Sci. Rep. 7 , 10936-10946 (2017).
Článok PubMed PubMed Central Študovňa Google
- Zhang, X., Zhu, Z., Xiang, N., Long, F. & Ni, Z. Automatizovaný mikrofluidný prístroj na bezznačkovú a vysokovýkonnú separáciu buniek. Anal. Chem. 90 , 4212 – 4220 (2018).
Článok CAS PubMed Študovňa Google
- Jia, Z. a kol. Jednobunková genetická analýza buniek pľúcneho nádoru založená na samoriadiacom mikrodutinovom čipe. Talanta 226 , 122172 (2021).
Článok CAS PubMed Študovňa Google
- Wang, J. a kol. Plne automatizovaný a integrovaný mikrofluidný systém na efektívnu detekciu CTC a jeho aplikáciu na skríning a prognózu hepatocelulárneho karcinómu. ACS Appl. Mater. Rozhrania 13 , 30174–30186 (2021).
Článok CAS PubMed Študovňa Google
- Lee, J. & Kwak, B. Simultánna izolácia na čipe a charakterizácia subpopulácií cirkulujúcich nádorových buniek. Biosens. Bioelektrón. 168 , 112564 (2020).
Článok CAS PubMed Študovňa Google
- Lee, AC a kol. OPENchip: platforma na molekulárne profilovanie in situ na čipe na analýzu génovej expresie a detekciu onkogénnych mutácií v jednotlivých cirkulujúcich nádorových bunkách. Lab Chip 20 , 912–922 (2020).
Článok CAS PubMed Študovňa Google
- Zhang, Y., Li, M., Gao, X., Chen, Y. & Liu, T. Nanotechnológia v diagnostike rakoviny: pokrok, výzvy a príležitosti. J. Hematol. Oncol. 12 , 137 (2019).
Článok PubMed PubMed Central Študovňa Google
- Jia, F. a kol. Nové magnetické nanočastice na báze peptidov na detekciu mezenchymálnych cirkulujúcich nádorových buniek. Anal. Chem. 93 , 5670-5675 (2021).
Článok CAS PubMed Študovňa Google
- Ding, P. a kol. Magnetické nanočastice funkcionalizované kyselinou tanínovou (TA) na izoláciu cirkulujúcich nádorových buniek (CTC) nezávislých od EpCAM od pacientov s rôznymi druhmi rakoviny. ACS Appl. Mater. Rozhrania 13 , 3694–3700 (2021).
Článok CAS PubMed Študovňa Google
- Li, F. a kol. Nedeštruktívne zachytávanie, uvoľňovanie a detekcia cirkulujúcich nádorových buniek pomocou magnetických nanosfér zdobených kyselinou listovou sprostredkovanou cystamínom. J. Mater. Chem. B 8 , 9971-9979 (2020).
Článok CAS PubMed Študovňa Google
- Vajhadin, F. a kol. Cytosenzor na báze MXene na detekciu HER2-pozitívnych rakovinových buniek pomocou magnetnanohybridov CoFe2O4@Ag konjugovaných s aptamérom HB5. Biosens. Bioelektrón. 195 , 113626 (2021).
- Wilson, RE a kol. Imunomagnetické zachytenie a detekcia multiplexných povrchových markerov cirkulujúcich nádorových buniek s magnetickými viacfarebnými povrchovo vylepšenými Ramanovými rozptylovými nanotagmi. ACS Appl. Mater. Rozhrania 12 , 47220–47232 (2020).
- Liu, S., Luo, J., Jiang, X., Li, X. & Yang, M. Nanovrstvy čierneho fosforu modifikované nanočasticami zlata so zlepšenou stabilitou na detekciu cirkulujúcich nádorových buniek. Mikrochim. Acta 187 , 397 (2020).
Článok CAS PubMed Študovňa Google
- Dou, B., Xu, L., Jiang, B., Yuan, R. & Xiang, Y. Aptamérom funkcionalizované a zlatým nanočasticovým poliom zdobené nanočastice magnetického grafénu umožňujú multiplexnú a citlivú elektrochemickú detekciu vzácnych cirkulujúcich nádorových buniek v celej krvi. Anal. Chem. 91 , 10792-10799 (2019).
Článok CAS PubMed Študovňa Google
- Sheng, W., Chen, T., Tan, W. & Fan, ZH Multivalentné nanosféry DNA na vylepšené zachytávanie rakovinových buniek v mikrofluidných zariadeniach. ACS Nano 7 , 7067-7076 (2013).
Článok CAS PubMed PubMed Central Študovňa Google
- Zhang, Y. a kol. Účinná synergická imunoterapia sprostredkovaná zlatými nanorúdkami na detekciu a inhibíciu pooperačnej recidívy nádoru. Acta Pharm. Sin. B 11 , 1978-1992 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Zhang, J. a kol. Citlivý signál zosilňujúci diagnostický biočip založený na biomimetickej periodickej nanoštruktúre na detekciu exozómov rakoviny. ACS Appl. Mater. Rozhrania 12 , 33473–33482 (2020).
Článok CAS PubMed Študovňa Google
- Cui, H. a kol. Rýchla a účinná izolácia a detekcia cirkulujúcich nádorových buniek na báze ZnS:Mn(2+) kvantových bodiek a magnetických nanokompozitov. Talanta 202 , 230–236 (2019).
Článok CAS PubMed Študovňa Google
- Yang, W. a kol. Reverzibilné zachytenie a voltametrické stanovenie cirkulujúcich nádorových buniek pomocou dvojrozmerného nanozýmu na báze PdMo zdobeného zlatými nanočasticami a aptamérom. Mikrochim. Acta 188 , 319 (2021).
Článok CAS PubMed Študovňa Google
- Su, Y. a kol. Protilátkový funkčný mikroguľôčkový filtračný čip s inerciálnym mikroprietokom na zachytenie veľkosti imunity a digitálnu detekciu cirkulujúcich nádorových buniek. ACS Appl Mater. Rozhrania 11 , 29569–29578 (2019).
Článok CAS PubMed Študovňa Google
- Husemann, Y. a kol. Systémové šírenie je skorým krokom pri rakovine prsníka. Cancer Cell 13 , 58-68 (2008).
- Hosseini, H. a kol. Včasné šírenie semien metastázuje pri rakovine prsníka. Príroda 540 , 552–558 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Rhim, AD a kol. Detekcia cirkulujúcich epiteliálnych buniek pankreasu u pacientov s cystickými léziami pankreasu. Gastroenterology 146 , 647-651 (2014).
- Yamaguchi, J. a kol. Premalígne pankreatické bunky vysievajú skryté metastázy vo vzdialených orgánoch u myší. Oncogene 40 , 2273-2284 (2021).
Článok CAS PubMed Študovňa Google
- Barrière, G., Riouallon, A., Renaudie, J., Tartary, M. & Rigaud, M. Mezenchymálne a kmeňové cirkulujúce nádorové bunky vo včasnej diagnostike rakoviny prsníka. BMC Cancer 12 , 114-120 (2012).
Článok PubMed PubMed Central Študovňa Google
- Thery, L. a kol. Cirkulujúce nádorové bunky v ranom štádiu prsníka. Cancer JNCI Cancer Spectr. 3 , pkz026 (2019).
- Paoletti, C. a kol. Zhluky cirkulujúcich nádorových buniek u pacientov s metastatickým karcinómom prsníka: štúdia translačnej medicíny SWOG S0500. Clin. Cancer Res 25 , 6089-6097 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Magbanua, MJM a kol. Synchrónna detekcia cirkulujúcich nádorových buniek v krvi a diseminovaných nádorových buniek v kostnej dreni predpovedá nepriaznivý výsledok vo včasnom štádiu rakoviny prsníka. Clin. Cancer Res. 25 , 5388-5397 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Magbanua, MJM a kol. Klinický význam cirkulujúcich nádorových buniek u pacientok s metastatickým karcinómom prsníka s pozitívnymi hormonálnymi receptormi, ktoré dostávali letrozol s bevacizumabom alebo bez neho. Clin. Cancer Res. 26 , 4911-4920 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Bortolini Silveira, A. a kol. Multimodálna tekutá biopsia na včasné monitorovanie a predikciu výsledku chemoterapie u metastatického karcinómu prsníka. NPJ Rakovina prsníka 7 , 115 (2021).
Článok PubMed PubMed Central Študovňa Google
- Paoletti, C. a kol. Počet cirkulujúcich nádorových buniek a index endokrinnej terapie u ER pozitívnych pacientov s metastatickým karcinómom prsníka. NPJ Rakovina prsníka 7 , 77 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Magbanua, MJM a kol. Sériová analýza cirkulujúcich nádorových buniek pri metastázujúcej rakovine prsníka, ktorá dostáva chemoterapiu prvej línie. J. Natl Cancer Inst. 113 , 443-452 (2021).
- de Kruijff, IE a kol. Vyčíslenie a charakterizácia cirkulujúcich nádorových buniek u pacientov s metastatickým karcinómom prostaty rezistentným na kastráciu liečených kabazitaxelom. Rakoviny 11 , 1212–1225 (2019).
Článok PubMed Central Študovňa Google
- Cieslikowski, WA a kol. Cirkulujúce nádorové bunky ako marker diseminovaného ochorenia u pacientov s novodiagnostikovaným vysokorizikovým karcinómom prostaty. Rakoviny 12 , 160–175 (2020).
Článok CAS PubMed Central Študovňa Google
- Basso, U. a kol. Prognostická úloha cirkulujúcich nádorových buniek pri metastatickom karcinóme obličky: veľká, multicentrická, prospektívna štúdia. Onkológ 26 , 740-750 (2021).
Článok PubMed PubMed Central Študovňa Google
- Chemi, F. a kol. Diseminácia pľúcnych venóznych cirkulujúcich nádorových buniek pred resekciou nádoru a relapsom ochorenia. Nat. Med 25 , 1534-1539 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Messaritakis, I. a kol. Charakterizácia DLL3-pozitívnych cirkulujúcich nádorových buniek (CTC) u pacientov s malobunkovým karcinómom pľúc (SCLC) a vyhodnotenie ich klinického významu počas liečby v prvej línii. Rakovina pľúc 135 , 33–39 (2019).
- Sun, YF a kol. Pooperačné cirkulujúce nádorové bunky: včasný prediktor extrahepatálnych metastáz u pacientov s hepatocelulárnym karcinómom podstupujúcich liečebnú chirurgickú resekciu. Rakovina Cytopathol. 128 , 733-745 (2020).
- Matsushita, D. a kol. Klinický význam cirkulujúcich nádorových buniek v odpovedi na trastuzumab na HER2-negatívny metastatický karcinóm žalúdka. Rakovina Chemother. Pharm. 87 , 789-797 (2021).
- Sastre, J. a kol. Spojenie medzi základnými cirkulujúcimi nádorovými bunkami, molekulárnym profilovaním nádoru a klinickými charakteristikami vo veľkej kohorte potenciálne zhromaždených chemo-naivných pacientov s metastatickým kolorektálnym karcinómom. Clin. Kolorektálny karcinóm 19 , e110–e116 (2020).
- Bidard, FC a kol. Cirkulujúce nádorové bunky u pacientov s rakovinou prsníka liečených neoadjuvantnou chemoterapiou: metaanalýza. J. Natl Cancer Inst. 110 , 560 – 567 (2018).
- Murlidhar, V. a kol. Zlá prognóza indikovaná zhlukmi žilových cirkulujúcich nádorových buniek v ranom štádiu rakoviny pľúc. CancerRes 77 , 5194-5206 (2017).
- Jansson, S., Bendahl, PO, Larsson, AM, Aaltonen, KE & Ryden, L. Prognostický vplyv celapoptózy cirkulujúceho nádoru a zhlukov v sériových vzorkách krvi od pacientov s metastatickým karcinómom prsníka v prospektívnej observačnej kohorte. BMC Cancer 16 , 433 (2016).
Článok PubMed PubMed Central Študovňa Google
- Wang, C. a kol. Pozdĺžne zozbierané CTC a CTC-klastre a klinické výsledky metastatického karcinómu prsníka. BreastCancer Res. Liečiť. 161 , 83-94 (2017).
- Wang, C. a kol. Zlepšená prognostická stratifikácia pomocou cirkulujúcich zhlukov nádorových buniek u pacientov s metastatickým karcinómom prostaty rezistentným na kastráciu. Cancers 13 , 268-280 (2021).
Článok CAS PubMed Central Študovňa Google
- Lozano, R. a kol. Hodnota včasnej dynamiky cirkulujúcich nádorových buniek na odhadnutie prínosu docetaxelu u pacientov s metastázujúcim karcinómom prostaty rezistentným na kastráciu (mCRPC). Cancers 13 , 2334–2344 (2021).
Článok PubMed PubMed Central Študovňa Google
- Su, P. a kol. Mezenchymálny a fosfatázový stav regenerácie pečene-3 v cirkulujúcich nádorových bunkách môže slúžiť ako rozhodujúci prognostický marker na hodnotenie relapsu alebo metastázy u pooperačných pacientov s kolorektálnym karcinómom. Clin. Prekl. Gastroenterol. 11 , e00265 (2020).
Článok PubMed PubMed Central Študovňa Google
- Strati, A., Nikolaou, M., Georgoulias, V. & Lianidou, ES Prognostický význam kvantifikácie transkriptov TWIST1, CD24, CD44 a ALDH1 v EpCAM-pozitívnych cirkulujúcich nádorových bunkách od pacientov s rakovinou prsníka v počiatočnom štádiu. Cells 8 , 652-667 (2019).
Článok CAS PubMed Central Študovňa Google
- Papadaki, MA a kol. Klinický význam imunitných kontrolných bodov na cirkulujúcich nádorových bunkách pri rakovine prsníka. Cancers 12 , 376-396 (2020).
Článok CAS PubMed Central Študovňa Google
- Wang, XQ, Liu, B., Li, BY, Wang, T. & Chen, DQ Vplyv CTC a hladiny INHBA na účinok a prognózu rôznych liečebných metód u pacientov s včasným karcinómom prsníka. Eur. Med. Pharm. Sci. 24 , 12735-12740 (2020).
- Graf, RP a kol. Klinická užitočnosť biomarkeru AR-V7 lokalizovaného v jadre v cirkulujúcich nádorových bunkách pri zlepšovaní výberu liečby lekárom pri rakovine prostaty rezistentnej na kastráciu. Eur. Urol. 77 , 170-177 (2020).
Článok CAS PubMed Študovňa Google
- Wei, T. a kol. Cirkulujúce nádorové bunky pozitívne na vimentín ako biomarker na diagnostiku a monitorovanie liečby u pacientov s rakovinou pankreasu. Cancer Lett. 452 , 237 – 243 (2019).
Článok CAS PubMed Študovňa Google
- Economos, C., Morrissey, C. & Vessella, RL Cirkulujúce nádorové bunky ako marker odpovede: dôsledky pre stanovenie účinnosti liečby a hodnotenie nových látok. Curr. Opin. Urol. 22 , 190-196 (2012).
- Li, Y., Wu, S. & Bai, F. Molekulárna charakterizácia cirkulujúcich nádorových buniek – od lavice po posteľ. Semin. Cell Dev. Biol. 75 , 88-97 (2018).
- Massard, C. a kol. Odpoveď RECIST a variácia cirkulujúcich nádorových buniek v štúdiách fázy 1: prospektívna multicentrická štúdia. Eur. J. Cancer 83 , 185-193 (2017).
- Ntzifa, A., Kotsakis, A., Georgoulias, V. & Lianidou, E. Detekcia mutácií EGFR v plazmatickej cfDNA a párových CTC pacientov s NSCLC pred a po liečbe osimertinibom pomocou kryštálovej digitálnej PCR. Cancers 13 , 2376-2394 (2021).
- Pan, X. & Zhang, X. Užitočnosť cirkulujúcich nádorových buniek a DNA pri liečbe pokročilého kolorektálneho karcinómu. FutureOncol 16 , 1289-1299 (2020).
- Garrido-Navas, MC a kol. Polemická diagnostická úloha mutácií tp53 v tekutých biopsiách z rakoviny prsníka, hrubého čreva a pľúc. Cancers 12 , 3343–3359 (2020).
Článok CAS PubMed Central Študovňa Google
- Mong, J. & Tan, MH Obohacovacie technológie založené na veľkosti pre nerakovinové bunky odvodené od nádoru v krvi. TrendsBiotechnol 36 , 511-522 (2018).
- Cristofanilli, M. a kol. Cirkulujúce nádorové bunky, progresia ochorenia a prežitie pri metastatickej rakovine prsníka. N. Engl. J. Med. 351 , 781-791 (2004).
Článok CAS PubMed Študovňa Google
- Liu, MC a kol. Cirkulujúce nádorové bunky: užitočný prediktor účinnosti liečby pri metastatickej rakovine prsníka. J. Clin. Oncol. 27 , 5153-5159 (2009).
Článok PubMed PubMed Central Študovňa Google
- Pestrin, M. a kol. Konečné výsledky multicentrickej klinickej štúdie fázy II hodnotiacej aktivitu jednozložkových pacientov s lapatinibom s HER2-negatívnym metastatickým karcinómom prsníka a HER2-pozitívnymi cirkulujúcimi nádorovými bunkami. Štúdia proof-of-concept. BreastCancer Res. Liečiť. 134 , 283-289 (2012).
- Pierga, JY a kol. Vysoká nezávislá prognostická a prediktívna hodnota cirkulujúcich nádorových buniek v porovnaní so sérovými nádorovými markermi vo veľkej prospektívnej štúdii v chemoterapii prvej línie u pacientov s metastatickým karcinómom prsníka. Ann. Oncol. 23, 618-624
- Giordano, A. a kol. Cirkulujúce nádorové bunky v imunohistochemických podtypoch metastatického karcinómu prsníka: nedostatok predpovedí pri HER2-pozitívnom ochorení liečenom cielenou terapiou. Ann. Oncol. 23 , 1144-1150 (2012).
Článok CAS PubMed Študovňa Google
- Jiang, ZF a kol. Cirkulujúce nádorové bunky predpovedajú celkové prežitie bez progresie u čínskych pacientov s metastatickým karcinómom prsníka, HER2-pozitívnym alebo trojito negatívnym (CBCSG004): multicentrická, dvojito zaslepená, prospektívna štúdia. Ann. Oncol. 24 , 2766-2772 (2013).
Článok CAS PubMed Študovňa Google
- Pierga, JY a kol. Cirkulujúce nádorové bunky a výsledok metastáz v mozgu u pacientov s HER2-pozitívnym karcinómom prsníka: štúdia LANDSCAPE. Ann. Oncol. 24 , 2999-3004 (2013).
- Smerage, JB a kol. Cirkulujúce nádorové bunky a odpoveď na chemoterapiu pri metastázujúcej rakovine prsníka: SWOG S0500. J. Clin. Oncol. 32 , 3483-3489 (2014).
Článok CAS PubMed PubMed Central Študovňa Google
- Hall, C. a kol. Cirkulujúce nádorové bunky po neoadjuvantnej chemoterapii v štádiu I-III triple-negatívnej rakoviny prsníka. Ann. Surg. Oncol. 22 , S552 – S558 (2015). Dodatok 3.
- Hall, CS a kol. Prognostická hodnota cirkulujúcich nádorových buniek identifikovaných pred chirurgickou resekciou u pacientok s nemetastatickým karcinómom prsníka. J. Am. Zb. Surg. 223 , 20-29 (2016).
Článok PubMed PubMed Central Študovňa Google
- Riethdorf, S. a kol. Prognostický vplyv cirkulujúcich nádorových buniek u pacientov s rakovinou prsníka liečených v neoadjuvantnej štúdii „geparquattro“. Clin. Cancer Res. 23 , 5384-5393 (2017).
Článok CAS PubMed Študovňa Google
- Sparano, J. a kol. Asociácia cirkulujúcich nádorových buniek s neskorou recidívou rakoviny prsníka s pozitívnym estrogénovým receptorom: sekundárna analýza randomizovanej klinickej štúdie. JAMA Oncol. 4 , 1700-1706 (2018).
Článok PubMed PubMed Central Študovňa Google
- Rossi, G. a kol. Bezbunková DNA a cirkulujúce nádorové bunky: komplexná analýza tekutej biopsie pri pokročilom karcinóme prsníka. Clin. Cancer Res. 24 , 560-568 (2018).
Článok CAS PubMed Študovňa Google
- Trapp, E. a kol. Prítomnosť cirkulujúcich nádorových buniek pri vysokorizikovej včasnej rakovine prsníka počas sledovania a prognózy. J. NatlCancer Inst. 111 , 380-387 (2019).
- Radovich, M. a kol. Asociácia cirkulujúcej nádorovej DNA a cirkulujúcich nádorových buniek po neoadjuvantnej chemoterapii s recidívou ochorenia u pacientov s trojnásobne negatívnym karcinómom prsníka: vopred plánovaná sekundárna analýza randomizovanej klinickej štúdie BRE12-158. JAMA Oncol. 6 , 1410-1415 (2020).
- Zhou, J. a kol. Stav epitelovo-mezenchymálneho prechodu cirkulujúcich nádorových buniek pri rakovine prsníka a jeho klinický význam. Cancer Biol. Med. 17 , 169-180 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Le, Du, F. a kol. EpCAM-nezávislá izolácia cirkulujúcich nádorových buniek s epitelovým-mezenchymálnym prechodom a fenotypmi rakovinových kmeňových buniek pomocou ApoStream® u pacientov s rakovinou prsníka liečených primárnou systémovou terapiou. PLoS One 15 , e0229903 (2020).
- Zhang, SR a kol. Mezenchymálny fenotyp cirkulujúcich nádorových buniek je spojený so vzdialenými metastázami u pacientov s rakovinou prsníka. Cancer Manag. Res. 9 , 691-700 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Bulfoni, M. a kol. U pacientok s metastatickým karcinómom prsníka je identifikácia cirkulujúcich nádorových buniek v epiteliálno-tomezenchymálnej transmisii spojená so zlou prognózou. Breast Cancer Res. 18 , 30 (2016).
Článok PubMed PubMed Central Študovňa Google
- Papadaki, MA a kol. Cirkulujúce nádorové bunky so stopkami a znakmi prechodu z epitelu na mezenchym sú chemorezistentné a predpovedajú zlý výsledok pri metastatickej rakovine prsníka. Mol. Cancer Ther. 18 , 437-447 (2019).
Článok CAS PubMed Študovňa Google
- de Kruijff, IE a kol. Expresia androgénneho receptora v cirkulujúcich nádorových bunkách pacientov s metastatickým karcinómom prsníka. Int. J. Cancer 145 , 1083-1089 (2019).
- Bock, C. a kol. Výrazná expresia cytokeratínu, N-kadherínu a CD133 v cirkulujúcich nádorových bunkách pacientov s metastatickým karcinómom prsníka. Budúci Oncol. 10 , 1751 – 1765 (2014).
Článok CAS PubMed Študovňa Google
- Goodman, OB a kol. Cirkulujúce nádorové bunky u pacientov so základnými hodnotami rakoviny prostaty rezistentnými na kastráciu a korelácia s prognostickými faktormi. Cancer Epidemiol. Biomark. Predch. 18 , 1904-1913 (2009).
- Goldkorn, A. a kol. Počty cirkulujúcich nádorových buniek sú prognózou celkového prežitia v SWOG S0421: štúdia fázy III s docetaxelom s atrasentanom alebo bez neho na metastatický karcinóm prostaty rezistentný na kastráciu. J. Clin. Oncol. 32 , 1136-113 (2014).
Článok CAS PubMed PubMed Central Študovňa Google
- Satelli, A. a kol. Potenciálna úloha expresie jadrového PD-L1 v cirkulujúcich nádorových bunkách pozitívnych na vimentín na bunkovom povrchu ako aprognostický marker u pacientov s rakovinou. Sci. Rep. 6 , 28910 (2016).
Článok CAS PubMed PubMed Central Študovňa Google
- Chen, J. a kol. Charakterizácia cirkulujúcich nádorových buniek pri rakovine prostaty založená na metabolickom preprogramovaní. J. Exp. Clin. Cancer Res. 37 , 127 (2018).
Článok PubMed PubMed Central Študovňa Google
- Liu, H., Ding, J., Wu, Y., Wu, D. & Qi, J. Prospektívna štúdia klinického vplyvu epiteliálnych a mezenchymálnych cirkulujúcich nádorových buniek v lokalizovanom karcinóme prostaty. Cancer Manag. Res. 12 , 4549-4560 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Antonarakis, ES a kol. AR-V7 a rezistencia na enzalutamid a abiraterón pri rakovine prostaty. N. Engl. J. Med. 371 , 1028-1038 (2014).
Článok PubMed PubMed Central Študovňa Google
- Okegawa, T. a kol. AR-V7 v cirkulujúcich nádorových bunkách sa zhlukuje ako prediktívny biomarker liečby abiraterón acetátom a enzalutamidom u pacientov s rakovinou prostaty rezistentnými na kastráciu. Prostata 78 , 576-582 (2018).
Článok CAS PubMed Študovňa Google
- Tagawa, ST a kol. Expresia AR-V7 a ARv(567es) v cirkulujúcich nádorových bunkách koreluje s výsledkami taxánovej terapie u mužov s metastatickým karcinómom prostaty liečených v TAXYNERGII. Clin. Cancer Res. 25 , 1880 – 1888 (2019).
Článok CAS PubMed Študovňa Google
- Markou, A. a kol. PIM-1 je nadmerne exprimovaný s vysokou frekvenciou v cirkulujúcich nádorových bunkách od pacientov s metastatickým karcinómom prostaty rezistentným na kastráciu. Cancers 12 , 1188-1201 (2020).
Článok CAS PubMed Central Študovňa Google
- Liu, S. a kol. Kombinované antigény karboanhydrázy 9 na povrchu buniek a CD147 umožňujú vysoko účinné zachytenie cirkulujúcich nádorových buniek u pacientov s čírymi bunkami s karcinómom obličky. Oncotarget 7 , 59877-59891 (2016).
Článok PubMed PubMed Central Študovňa Google
- Naoe, M. a kol. Detekcia cirkulujúcich urotelových rakovinových buniek v krvi pomocou systému CellSearch. Cancer 109 , 1439-1445 (2007).
- Gallagher, DJ a spol. Detekcia cirkulujúcich nádorových buniek u pacientov s uroteliálnym karcinómom. Ann. Oncol. 20 , 305-308 (2009).
Článok CAS PubMed Študovňa Google
- Rink, M. a kol. Detekcia cirkulujúcich nádorových buniek v periférnej krvi pacientov s pokročilým nemetastatickým karcinómom močového mechúra. BJU Int. 107 , 1668 – 1675 (2011).
- Gazzaniga, P. a kol. Prognostická hodnota cirkulujúcich nádorových buniek pri nesvalovej invazívnej rakovine močového mechúra: analýza CellSearch. Ann. Oncol. 23 , 2352-2356 (2012).
Článok CAS PubMed Študovňa Google
- Cohen, SJ a kol. Vzťah cirkulujúcich nádorových buniek k nádorovej odpovedi, prežívaniu bez progresie a celkovému prežívaniu hospitalizovaných pacientov s metastatickým kolorektálnym karcinómom. J. Clin. Oncol. 26 , 3213-3221 (2008).
- Cohen, SJ a kol. Prognostický význam cirkulujúcich nádorových buniek u pacientov s metastatickým kolorektálnym karcinómom. Ann. Oncol. 20 , 1223-1229 (2009).
Článok CAS PubMed Študovňa Google
- Wang, W. a kol. Hladiny mezenchymálneho markera a expresie LGR5 v cirkulujúcich nádorových bunkách korelujú s prognózou kolorektálneho karcinómu. Cell Oncol. 41 , 495-504 (2018).
- Wu, F. a kol. Asociácie medzi epitelovo-mezenchymálnymi prechodnými fenotypmi cirkulujúcich nádorových buniek a klinickopatologickými znakmi pacientov s kolorektálnym karcinómom. Dis. Markers 2017 , 9474532 (2017).
Článok PubMed PubMed Central Študovňa Google
- Zhao, R. a kol. Expresia a klinický význam epiteliálnych a mezenchymálnych markerov v cirkulujúcich nádorových bunkách z kolorektálneho karcinómu. Oncotarget 8 , 9293-9302 (2017).
- Ning, Y. a kol. Klinický význam expresie EMT a kmeňového génu v cirkulujúcich nádorových bunkách u pacientov s metastatickým kolorektálnym karcinómom. Farmakogenom. J. 18 , 29-34 (2018).
- Bao, H. a kol. Vysoká expresia karcinoembryonálneho antigénu a telomerázovej reverznej transkriptázy v cirkulujúcich nádorových bunkách je spojená so slabou klinickou odpoveďou na inhibítor imunitného kontrolného bodu nivolumab. Oncol. Lett. 15 , 3061-3067 (2018).
- Shen, C., Hu, L., Xia, L. & Li, Y. Kvantitatívna detekcia RT-PCR v reálnom čase pre survivín, CK20 a CEA v periférnej krvi pacientov s kolorektálnym karcinómom. Jpn. J. Clin. Oncol. 38 , 770-776 (2008).
- Shimada, R., Iinuma, H., Akahane, T., Horiuchi, A. & Watanabe, T. Prognostický význam CTC a CSC krvnej drenážnej žily u pacientov s kolorektálnym karcinómom v štádiu B a C podľa Dukesa. Oncol. Rep. 27 , 947-953 (2012).
Článok PubMed PubMed Central Študovňa Google
- Barbazan, J. a kol. Multimarkerový panel na detekciu cirkulujúcich nádorových buniek predpovedá výsledok AQ5 pacienta a odpoveď na liečbu pri metastatickom kolorektálnom karcinóme. Int. J. Cancer 135 , 2633-2643 (2014).
Článok CAS PubMed Študovňa Google
- Yokobori, T. a kol. Plastin3 je nový marker pre cirkulujúce nádorové bunky, ktoré prechádzajú epiteliálno-mezenchymálnym prechodom a je spojený s prognózou kolorektálneho karcinómu. Cancer Res. 73 , 2059-2069 (2013).
Článok CAS PubMed Študovňa Google
- Bian, J., Yan, K., Liu, N. & Xu, X. Korelácie medzi fenotypizáciou cirkulujúcich nádorových buniek a absorpciou 18F-fluórdeoxyglukosepozitrónovej emisnej tomografie pri nemalobunkovom karcinóme pľúc. J. Cancer Res. Clin. Oncol. 146 , 2621 – 2630 (2020).
Článok CAS PubMed Študovňa Google
- Dong, J. a kol. Detekcia molekulárneho podtypu cirkulujúcich nádorových buniek v pľúcnej žile predpovedajúca prognózu pacientov s nemalobunkovým karcinómom pľúc v štádiu I-III. Predný Oncol. 9 , 1139 (2019).
Článok PubMed PubMed Central Študovňa Google
- Manjunath, Y. a kol. Expresia PD-L1 s epiteliálnym mezenchymálnym prechodom cirkulujúcich nádorových buniek je spojená so slabým prežitím pri kuratívne resekovanom nemalobunkovom karcinóme pľúc. Cancers 11 , 806-816 (2019).
Článok CAS PubMed Central Študovňa Google
- Krebs, MG a kol. Hodnotenie a prognostický význam cirkulujúcich nádorových buniek u pacientov s nemalobunkovým karcinómom pľúc. J. Clin. Oncol. 29 , 1556-1563 (2011).
- Punnoose, EA a kol. Hodnotenie cirkulujúcich nádorových buniek a cirkulujúcej nádorovej DNA pri nemalobunkovom karcinóme pľúc: spojenie s klinickými koncovými bodmi v klinickej štúdii fázy II s pertuzumabom a erlotinibom. Clin. Cancer Res. 18 , 2391-2401 (2012).
Článok CAS PubMed Študovňa Google
- Liang, N. a kol. Efektívna izolácia a kvantifikácia cirkulujúcich nádorových buniek u pacientov s nemalobunkovým karcinómom pľúc pomocou magnetických nanočastíc funkcionalizovaných peptidom. J. Thorac. Dis. 12 , 4262-4273 (2020).
Článok PubMed PubMed Central Študovňa Google
- Tamminga, M. a kol. Cirkulujúce nádorové bunky u pacientov s pokročilou nemalobunkovou rakovinou pľúc sú spojené s horšou odpoveďou nádoru na inhibítory kontrolných bodov. J. Immunother. Rakovina 7 , 173 (2019).
Článok PubMed PubMed Central Študovňa Google
- Tamminga, M. a kol. Analýza uvoľnených cirkulujúcich nádorových buniek počas chirurgického zákroku pre nemalobunkový karcinóm pľúc. Clin. CancerRes. 26, 1656 – 1666 (2020).
- Frick, MA a kol. Cirkulujúce nádorové bunky sú spojené s rekurentným ochorením u pacientov s nemalobunkovým karcinómom v počiatočnom štádiu liečených stereotaktickou rádioterapiou tela. Clin. Cancer Res. 26 , 2372-2380 (2020).
Článok CAS PubMed Študovňa Google
- Hiltermann, TJN a kol. Cirkulujúce nádorové bunky pri malobunkovom karcinóme pľúc: prediktívny a prognostický faktor. Ann. Oncol. 23 , 2937-2942 (2012).
Článok CAS PubMed Študovňa Google
- Hou, JM a kol. Hodnotenie cirkulujúcich nádorových buniek a biomarkerov sérologickej bunkovej smrti u pacientov s malobunkovým karcinómom pľúc, ktorí podstupujú chemoterapiu. Am. J. Pathol. 175 , 808-816 (2009).
Článok CAS PubMed PubMed Central Študovňa Google
- Hou, JM a kol. Klinický význam a molekulárne charakteristiky cirkulujúcich nádorových buniek a cirkulujúcich nádorových mikroembólií u pacientov s malobunkovým karcinómom pľúc. J. Clin. Oncol. 30 , 525-532 (2012).
- Huang, CH a kol. Multicentrická pilotná štúdia skúmajúca úlohu cirkulujúcich nádorových buniek ako krvných nádorových markerov u pacientov s rozsiahlym malobunkovým karcinómom pľúc. Predný Oncol. 4 , 271 (2014).
Článok PubMed PubMed Central Študovňa Google
- Naito, T. a kol. Prognostický vplyv cirkulujúcich nádorových buniek u pacientov s malobunkovým karcinómom pľúc. J. Thorac. Oncol. 7 , 512-519 (2012).
- Normanno, N. a kol. Prognostická hodnota zníženia cirkulujúcich nádorových buniek u pacientov s rozsiahlym malobunkovým karcinómom pľúc. Rakovina pľúc 85 , 314-319 (2014).
- Messaritakis, I. a kol. Fenotypová charakterizácia cirkulujúcich nádorových buniek v periférnej krvi pacientov s malobunkovým karcinómom. PLoS One 12 , e0181211 (2017).
Článok PubMed PubMed Central Študovňa Google
- Bidard, FC a kol. Cirkulujúce nádorové bunky pri lokálne pokročilom adenokarcinóme pankreasu: doplnková štúdia CirCe 07 k štúdii LAP 07. Ann. Oncol. 24 , 2057-2061 (2013).
Článok CAS PubMed Študovňa Google
- Súd, CM a spol. Cirkulujúce nádorové bunky predpovedajú okultné metastatické ochorenie a prognózu pri rakovine pankreasu. Ann. Surg. Oncol. 25 , 1000-1008 (2018).
Článok PubMed PubMed Central Študovňa Google
- Gall, TM a kol. Znížená diseminácia cirkulujúcich nádorových buniek s bezdotykovou chirurgickou technikou u pacientov s rakovinou pankreasu. JAMA Surg. 149 , 482-485 (2014).
- Hugenschmidt, H. a kol. Cirkulujúce nádorové bunky sú nezávislým prediktorom kratšieho prežitia u pacientov podstupujúcich resekciu pre pankreatický a periampulárny adenokarcinóm. Ann. Surg. 271 , 549-558 (2020).
- Okubo, K. a kol. Klinický vplyv cirkulujúcich nádorových buniek a odpoveď na liečbu pri rakovine pankreasu. Eur. J. Surg. Oncol. 43 , 1050-1055 (2017).
- Dong, X. a kol. Priestorová heterogenita v epiteliálnych a mezenchymálnych prechodových vlastnostiach cirkulujúcich nádorových buniek spojených so vzdialenou recidívou u pacientov s rakovinou pankreasu. Ann. Prekl. Med. 8 , 676 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Zhao, XH a kol. Molekulárna detekcia epitelovo-mezenchymálnych prechodových markerov v cirkulujúcich nádorových bunkách od pacientov s rakovinou pankreasu: Potenciálna úloha v klinickej praxi. World J. Gastroenterol. 25 , 138-150 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Zhu, P. a kol. Cirkulujúce nádorové bunky exprimujúce Kruppel-like faktor 8 a vimentín ako prediktory zlej prognózy pacientov s rakovinou pankreasu. Cancer Control 28 , 10732748211027163 (2021).
Článok PubMed PubMed Central Študovňa Google
- Ou, H. a kol. Fenotyp cirkulujúcich nádorových buniek naznačuje slabé prežitie a recidívu po operácii hepatocelulárneho karcinómu. Dig. Dis. Sci. 63 , 2373-2380 (2018).
Článok CAS PubMed Študovňa Google
- Wang, PX a kol. Cirkulujúce nádorové bunky sú indikátorom na podávanie adjuvantnej transarteriálnej chemoembolizácie pri hepatocelulárnom karcinóme: retrospektívna štúdia s jedným centrom, ktorá zodpovedá sklonu. Clin. Prekl. Med. 10 , e137 (2020).
Článok PubMed PubMed Central Študovňa Google
- Yu, JJ a kol. Účinok chirurgickej resekcie pečene na cirkulujúce nádorové bunky u pacientov s hepatocelulárnym karcinómom. BMCCancer 18 , 835 (2018).
- Zhou, J. a kol. Predoperačné cirkulujúce nádorové bunky na predpovedanie mikrovaskulárnej invázie a dynamická detekcia naznačujú prognózu hepatocelulárneho karcinómu. BMC Cancer 20 , 1047 (2020).
Článok PubMed PubMed Central Študovňa Google
- Zhou, KQ a kol. Vplyv chirurgického okraja na recidívu na základe predoperačného stavu cirkulujúcich nádorových buniek v hepatocelulárnom karcinóme. EBioMedicine 62 , 103107 (2020).
Článok PubMed PubMed Central Študovňa Google
- Liu, YK a kol. Vylepšená stratégia na detekciu procesu epitelovo-mezenchymálneho prechodu u cirkulujúcich nádorových buniek u pacientov s hepatocelulárnym karcinómom. Hepatol. Int 10 , 640-646 (2016).
- Qi, LN a kol. Cirkulujúce nádorové bunky podstupujúce EMT poskytujú metriku pre diagnostiku a prognózu pacientov s hepatocelulárnym karcinómom. Cancer Res. 78 , 4731-4744 (2018).
Článok CAS PubMed Študovňa Google
- Wang, Z. a kol. Korelácia medzi pooperačnou skorou recidívou hepatocelulárneho karcinómu a mezenchymálnymi cirkulujúcimi nádorovými bunkami v periférnej krvi. J. Gastrointest. Surg. 22 , 633-639 (2018).
- Súd, CM a spol. Nový multimarkerový test na fenotypové profilovanie cirkulujúcich nádorových buniek pri hepatocelulárnom karcinóme. Transpl. 24 , 946-960 (2018).
Článok PubMed PubMed Central Študovňa Google
- Yi, B. a kol. Klinický význam obohatenia CTC pomocou GPC3-IML a jeho genetická analýza pri hepatocelulárnom karcinóme. J. Nanobiotechnol. 19 , 74 (2021).
- Sun, YF a kol. Rozoberanie priestorovej heterogenity a mechanizmu imunitného úniku CTC pomocou jednobunkového RNA-seq inhepatocelulárneho karcinómu. Nat. komun. 12 , 4091 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Yin, LC a kol. Twist expresia v cirkulujúcich bunkách hepatocelulárneho karcinómu predpovedá metastázy a prognózy. Biomed. Res. Medzinárodný rok 2018 , 3789613 (2018).
Článok PubMed PubMed Central Študovňa Google
- Sun, YF a kol. Cirkulujúce nádorové bunky s adhéziou epitelových buniek podobných kmeňovým bunkám indikujú zlú prognózu hepatocelulárneho karcinómu po kuratívnej resekcii. Hepatology 57 , 1458-1468 (2013).
Článok CAS PubMed Študovňa Google
- Lee, SJ a kol. Cirkulujúce nádorové bunky predpovedajú slabú odpoveď na chemoterapiu pri metastatickej rakovine žalúdka. Int. J. Biol. Markers 30 , e382–e386 (2015).
- Uenosono, Y. a kol. Klinický význam cirkulujúcich nádorových buniek v periférnej krvi od pacientov s rakovinou žalúdka. Cancer 119 , 3984-3991 (2013).
- Zhang, Q. a kol. Prospektívna štúdia zmien a klinického významu predoperačných a pooperačných cirkulujúcich nádorových buniek pri resekovateľnom karcinóme žalúdka. J. Transl. Med. 16 , 171 (2018).
Článok CAS PubMed PubMed Central Študovňa Google
- Liu, M. a kol. Prognostický význam expresie PD-L1 na cirkulujúcich nádorových bunkách pozitívnych na vimentín na bunkovom povrchu u pacientov s rakovinou žalúdka. Mol. Oncol. 14 , 865-881 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Hatakeyama, K. a kol. Nový zostrihový variant XIAP-asociovaného faktora 1 (XAF1) je exprimovaný v cirkulujúcich nádorových bunkách odvodených od rakoviny žalúdka s periférnou krvou. Gastr. Cancer 18 , 751-761 (2015).
- Vaiopoulos, AG a kol. Detekcia cirkulujúcich nádorových buniek pri kolorektálnom a žalúdočnom karcinóme pomocou multiplexného PCR testu. Anticancer Res. 34 , 3083-3092 (2014).
- Ishiguro, Y. a kol. Prognostický význam cirkulujúcich nádorových buniek s mezenchymálnymi fenotypmi u pacientov s rakovinou žalúdka: prospektívna štúdia. Ann. Surg. Oncol. 28 , 1178-1186 (2021).
- Mimori, K. a kol. Rozsiahla štúdia MT1-MMP ako markera pre izolované nádorové bunky v periférnej krvi a kostnej dreni v prípadoch rakoviny žalúdka. Ann. Surg. Oncol. 15 , 2934-2942 (2008).
- Li, Y. a kol. Prognostická hodnota cirkulujúcich nádorových buniek detegovaných systémom CellSearch u pacientov s rakovinou pažeráka: asystematický prehľad a metaanalýza. BMC Cancer 20 , 581 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Tewari, KS a kol. Cirkulujúce nádorové bunky pri pokročilom karcinóme krčka maternice: NRG onkologicko-gynekologická onkologická skupinová štúdia240 (NCT 00803062). Mol. Cancer Ther. 19 , 2363-2370 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Anand, K. a kol. Pilotná štúdia cirkulujúcich nádorových buniek v počiatočnom štádiu a metastatickom uveálnom melanóme. Cancers 11 , 856-863 (2019).
Článok CAS PubMed Central Študovňa Google
- Kim, DD, Yang, CS, Chae, HD, Kwak, SG & Jeon, CH Člen génovej rodiny A1-6 a hTERT kódujúci melanómový antigén pri detekcii cirkulujúcich nádorových buniek po deplécii CD45 (-) a extrakcii RNA. Oncol. Lett. 14 , 837-843 (2017).
Článok CAS PubMed PubMed Central Študovňa Google
- Mego, M. a kol. Cirkulujúce nádorové bunky s fenotypmi epitelového-mezenchymálneho prechodu spojenými s horšími výsledkami pri primárnej rakovine prsníka. Anticancer Res. 39 , 1829-1837 (2019).
Článok CAS PubMed Študovňa Google
- Zhang, Y. a kol. Využiteľnosť cirkulujúcich nádorových buniek na detekciu skorého štádia luminálnej rakoviny prsníka. Am. J. Med Sci. 360 , 543 – 551 (2020).
- Štefanovič, S. a kol. Nedostatok dôkazov o súvislosti medzi vzormi konverzie biomarkerov rakoviny a stavom CTC u pacientov s metastatickým karcinómom prsníka. Int. J. Mol. Sci. 21 , 2161-2171 (2020).
Článok PubMed Central Študovňa Google
- Jin, L. a kol. Hodnotenie diagnostickej hodnoty cirkulujúcich nádorových buniek so systémom zachytávania CTC CytoSorter((R)) u pacientov s rakovinou prsníka. Cancer Med. 9 , 1638-1647 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Shliakhtunou, YA CTC-orientovaná adjuvantná personalizovaná cytostatická terapia pacienti s nemetastatickým karcinómom prsníka: kontinuálna nerandomizovaná prospektívna štúdia a prospektívna randomizovaná kontrolovaná štúdia. Breast Cancer Res. Liečiť. 186 , 439-451 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Sieuwerts, AM a kol. Varianty zostrihu AR v cirkulujúcich nádorových bunkách pacientov s rakovinou prostaty rezistentnou na kastráciu: vzťah s výsledkom kabazitaxelu. Mol. Oncol. 13 , 1795-1807 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Schonhoft, JD a kol. Morfologicky predpovedaný počet prechodov vo veľkom meradle v cirkulujúcich nádorových bunkách identifikuje biomarker achromozomálnej nestability spojený so zlým výsledkom pri rakovine prostaty rezistentnej na kastráciu. Cancer Res. 80 , 4892-4903 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Armstrong, AJ a kol. Prospektívna multicentrická štúdia cirkulujúcich nádorových buniek AR-V7 a taxánu verzus výsledky hormonálnej liečby u metastatického karcinómu prostaty rezistentného na kastráciu. JCO Precis. Oncol. 4 , 1285-1301 (2020).
- Xu, L. a kol. Neinvazívna detekcia klinicky významnej rakoviny prostaty pomocou cirkulujúcich nádorových buniek. J. Urol. 203 , 73-82 (2020).
- Sperger, JM a kol. Prospektívne hodnotenie klinických výsledkov pomocou multiplexnej tekutej biopsie zameranej na rôzne mechanizmy rezistencie pri metastatickej rakovine prostaty. J. Clin. Oncol. 39 , 2926-2937 (2021).
- Zhang, P. a kol. Význam detekcie cirkulujúcich nádorových buniek a BECLIN1 v periférnej krvi pacientov s renálnym bunkovým karcinómom. Crit. Eukaryot. Gene Expr. 30 , 483-492 (2020).
- Li, Z. a kol. Cirkulujúce nádorové bunky môžu predpovedať prognózu pacientov s nemalobunkovým karcinómom pľúc po resekcii: aretrospektívna štúdia. Prekl. Lung Cancer Res 10 , 995-1006 (2021).
Článok CAS PubMed PubMed Central Študovňa Google
- Wang, PP a kol. Cirkulujúce nádorové bunky ako nový prediktívny a prognostický faktor u pacientov s malobunkovým karcinómom pľúc. J. Cancer 11 , 2113-2122 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Ha, Y. a kol. Cirkulujúce nádorové bunky sú spojené so zlými výsledkami v počiatočnom štádiu hepatocelulárneho karcinómu: aprospektívna štúdia. Hepatol. Int. 13 , 726-735 (2019).
- Chen, Y. a kol. Cirkulujúce nádorové bunky podstupujúce EMT slabo korelujú s klinickými štádiami alebo predpovedajú recidívu hepatocelulárneho karcinómu. Sci. Rep. 9 , 7084 (2019).
Článok PubMed PubMed Central Študovňa Google
- Cheng, Y. a kol. Diagnostická hodnota rôznych fenotypových cirkulujúcich nádorových buniek v hepatocelulárnom karcinóme. J. Gastrointest. Surg. 23 , 2354-2361 (2019).
- Lei, Y. a kol. Asociácia predoperačných hladín NANOG-pozitívnych cirkulujúcich nádorových buniek s recidívou hepatocelulárneho karcinómu. Predné. Oncol. 11 , 601668 (2021).
Článok PubMed PubMed Central Študovňa Google
- Szczepanik, A. a kol. CD44(+) cytokeratín-pozitívne nádorové bunky v krvi a kostnej dreni sú spojené so zlou prognózou pacientov s rakovinou žalúdka. Gastr. Rakovina 22 , 264–272 (2019).
- Miki, Y. a kol. Cirkulujúce CEA-pozitívne a EpCAM-negatívne nádorové bunky môžu byť prediktívnym biomarkerom pre pacientov s recidívou rakoviny žalúdka. Cancer Med. 10 , 521-528 (2021).
Článok CAS PubMed Študovňa Google
- Kuroda, K. a kol. Cirkulujúce nádorové bunky s expresiou FGFR2 môžu byť užitočné na identifikáciu pacientov s existujúcim nádorom nadmerne exprimujúcim FGFR2. Cancer Sci. 111 , 4500-4509 (2020).
Článok CAS PubMed PubMed Central Študovňa Google
- Wang, D. a kol. Prognostické modely založené na pooperačných cirkulujúcich nádorových bunkách môžu predpovedať slabé prežívanie bez recidívy nádoru u pacientov s kolorektálnym karcinómom štádia II-III. J. Cancer 10 , 4552-4563 (2019).
Článok CAS PubMed PubMed Central Študovňa Google
- Bidard, FC a kol. Cirkulujúce nádorové bunky a detekcia cirkulujúcej nádorovej DNA pri potenciálne resekovateľnom metastatickom kolorektálnom karcinóme: prospektívna doplnková štúdia k jednorakovinovej štúdii Prodige-14. Cells 8 , 516-528 (2019).
Článok CAS PubMed Central Študovňa Google
- Wang, L. a kol. Cirkulujúce nádorové bunky ako nezávislý prognostický faktor pri pokročilom kolorektálnom karcinóme: retrospektívna štúdia u 121 pacientov. Int. J. Colorectal Dis. 34 , 589-597 (2019).
- Messaritakis, I. a kol. Hodnotenie úlohy cirkulujúcich nádorových buniek a stavu nestability mikrosatelitov pri predpovedaní výsledku u pacientov s pokročilým CRC. J. Pers. Med. 10 , 235-347 (2020).
Článok PubMed Central Študovňa Google
- Pan, RJ a kol. Detekcia a klinická hodnota cirkulujúcich nádorových buniek ako asistovaného prognostického markera u pacientov s kolorektálnym karcinómom. Cancer Manag. Res. 13 , 4567-4578 (2021).
Článok PubMed PubMed Central Študovňa Google
Financovanie
Táto štúdia bola podporená financovaním Národnej nadácie pre prírodné vedy v Číne (Grant č. 82172344, 81702866, Jiaojiao Zhou), Nadácia prírodných vied v provincii Zhejiang (Grant č. LY21H160039, Jiaojiao Zhou), Fundamental Universities Research Funds for the Central Universities Research Funds (Grant č. 2021FZJD009, Jiaojiao Zhou) a Národná nadácia pre prírodné vedy Číny (Grant č. 82072900, Yiding Chen).
Informácie o autorovi
Poznámky autora
- Títo autori prispeli rovnakým dielom: Danfeng Lin, Lesang Shen, Meng Luo a Kun Zhang
Autori a príslušnosti
- Oddelenie chirurgie prsníka, Druhá pridružená nemocnica, Zhejiang University School of Medicine, Hangzhou, Čína
Danfeng Lin, Lesang Shen, Meng Luo, Kun Zhang, Fangfang Zhu, Shu Zheng, Yiding Chen & Jiaojiao Zhou
- Cancer Institute (Kľúčové laboratórium prevencie a intervencie rakoviny, Čínske národné ministerstvo školstva), Druhá pridružená nemocnica, Lekárska fakulta univerzity Zhejiang, Hangzhou, Čína
Danfeng Lin, Meng Luo, Shu Zheng, Yiding Chen & Jiaojiao Zhou
- Oddelenie chirurgie prsníka, Prvá pridružená nemocnica lekárskej univerzity Wenzhou, Wenzhou, Čína
Danfeng Lin
- Katedra patológie, Druhá pridružená nemocnica, Lekárska fakulta univerzity Zhejiang, Hangzhou, Čína
Jinfan Li a Qi Yang
- Chirurgické oddelenie, Tradičná čínska lekárska nemocnica Zhuji, Shaoxing, Čína
Dan Zhou
Zodpovedajúci autori
Korešpondencia s Yiding Chen alebo Jiaojiao Zhou .
Etické vyhlásenia
Konkurenčné záujmy
Autori nedeklarujú žiadne konkurenčné záujmy.
Práva a povolenia
Otvorený prístup Tento článok je licencovaný na základe medzinárodnej licencie Creative Commons Attribution 4.0, ktorá povoľuje používanie, zdieľanie, adaptáciu, distribúciu a reprodukciu na akomkoľvek médiu alebo formáte, ak uvediete pôvodného autora (autorov) a zdroj, uveďte odkaz na licenciu Creative Commons a uveďte, či boli vykonané zmeny. Obrázky alebo iné materiály tretích strán v tomto článku sú zahrnuté v licencii Creative Commons k článku, pokiaľ nie je v úverovom limite k materiálu uvedené inak. Ak materiál nie je zahrnutý v licencii Creative Commons k článku a vaše zamýšľané použitie nie je povolené zákonnými predpismi alebo prekračuje povolené použitie, budete musieť získať povolenie priamo od držiteľa autorských práv. Ak chcete zobraziť kópiu tejto licencie, navštívte stránku http://creativecommons.org/licenses/by/4.0/ .
O tomto článku
Citujte tento článok
Lin, D., Shen, L., Luo, M. a kol. Cirkulujúce nádorové bunky: biológia a klinický význam. Sig Transduct Target Ther 6 , 404 (2021). https://doi.org/10.1038/s41392-021-00817-8
- Prijaté13. júla 2021
- Prepracované6. októbra 2021
- Prijaté27. októbra 2021
- Zverejnené22. novembra 2021
- DOIhttps://doi.org/10.1038/s41392-021-00817-8
Zdieľajte tento článok
Každý, s kým zdieľate nasledujúci odkaz, si bude môcť prečítať tento obsah:
Získajte odkaz na zdieľanie
Poskytuje iniciatíva Springer Nature SharedIt na zdieľanie obsahu
Predmety
Tento článok cituje
- Biomarkery založené na krvi u pacientov s nemalobunkovým karcinómom pľúc liečených blokádou imunitného kontrolného bodu
- Yo-Ting Tsai
- Jeffrey Schlom
- Renee N. Donahue
Journal of Experimental & Clinical Cancer Research (2024)
- Biosenzory SERS pre tekutú biopsiu na diagnostiku rakoviny detekciou rôznych cirkulujúcich biomarkerov: súčasný pokrok a perspektívy
- Nana Lyu
- Amin Hassanzadeh-Barforoushi
- Yuling Wang
Nano konvergencia (2024)
- Prípad odpovede na kombinovanú liečbu s TSA-DC-CTL imunoterapiou a osimertinibom pri EGFR mutovanom pokročilom pľúcnom adenokarcinóme
- Zhiyi Han
- Tao Li
- Tongmei Zhang
Molekulárna rakovina (2024)
- Techniky tekutej biopsie a rakovina pľúc: diagnostika, monitorovanie a hodnotenie
- Fei Ren
- Qian Fei
- Lei Sun
Journal of Experimental & Clinical Cancer Research (2024)
Journal of Analytical Science and Technology (2024)
- Sekcie
- Figúrky
- Referencie
- Abstraktné
- Úvod
- Biológia CTC
- CTC a krvné mikroprostredie
- Technológie na obohacovanie a izoláciu CTC
- Klinické aplikácie CTC
- Diskusia
- Referencie
- Financovanie
- Informácie o autorovi
- Etické vyhlásenia
- Práva a povolenia
- O tomto článku
- Tento článok cituje
Transdukcia signálu a cielená terapia ( Sig Transduct Target Ther ) ISSN 2059-3635 (online)
